近期,上海大学转化医学研究院/上海交通大学医学院附属新华医院骨科苏佳灿教授团队在期刊 Military Medical Research 上发表综述究性文章:"Accelerating Cartilage Regeneration with DNA-SF Hydrogel Sustained Release System-Based Cartilage Organoids"。文章将“共价缓释 + 3D打印”整合进类器官工程,在4周内稳定塑造透明软骨表型并在8周内实现功能性修复。它把材料的长期供能与分化信号的时序调控打通,为长期培养的类器官移植提供了可标准化的材料-类器官协同路径。转录组-通路-蛋白多层证据链支撑MAPK为关键轴,具备向临床修复/药筛/疾病模型延展的潜力。上海大学转化医学研究院沈聪昳博士研究生、武翔博士研究生、韩欣雨硕士研究生、上海交通大学医学院附属新华医院周启荣主治医师为论文共同第一作者,上海大学转化医学研究院/上海交通大学医学院附属新华医院苏佳灿教授、上海大学转化医学研究院耿振副研究员、上海交通大学医学院附属新华医院王成龙副主任医师、王建华主任医师为论文共同通讯作者。

研究背景
软骨修复在再生医学中仍是难题。尽管近年来用于软骨修复的生物材料研究繁多,但仍存在修复周期长与疗效欠佳等问题。类器官是由干/祖细胞定向分化形成的微型三维组织,能够模拟天然器官的结构与功能,因此构建软骨类器官(COs)被认为是软骨修复的有前景策略。
本研究旨在通过构建毫米级软骨类器官来修复软骨缺损。首先,课题组利用丙烯酰化聚乙二醇NHS酯将氨糖(促软骨基质合成)和TD-198946(促软骨分化)共价接枝到DNA-SF水凝胶中制备了DNA-SF缓释水凝胶(DSRGT)。通过测定DSRGT对BMSCs软骨分化的促进作用,验证了其作为长期培养软骨类器官的潜力。利用DLP系统将BMSCs与DSRGT混合打印成毫米级球体,并在体外诱导培养2至6周,成功构建了毫米级软骨类器官。
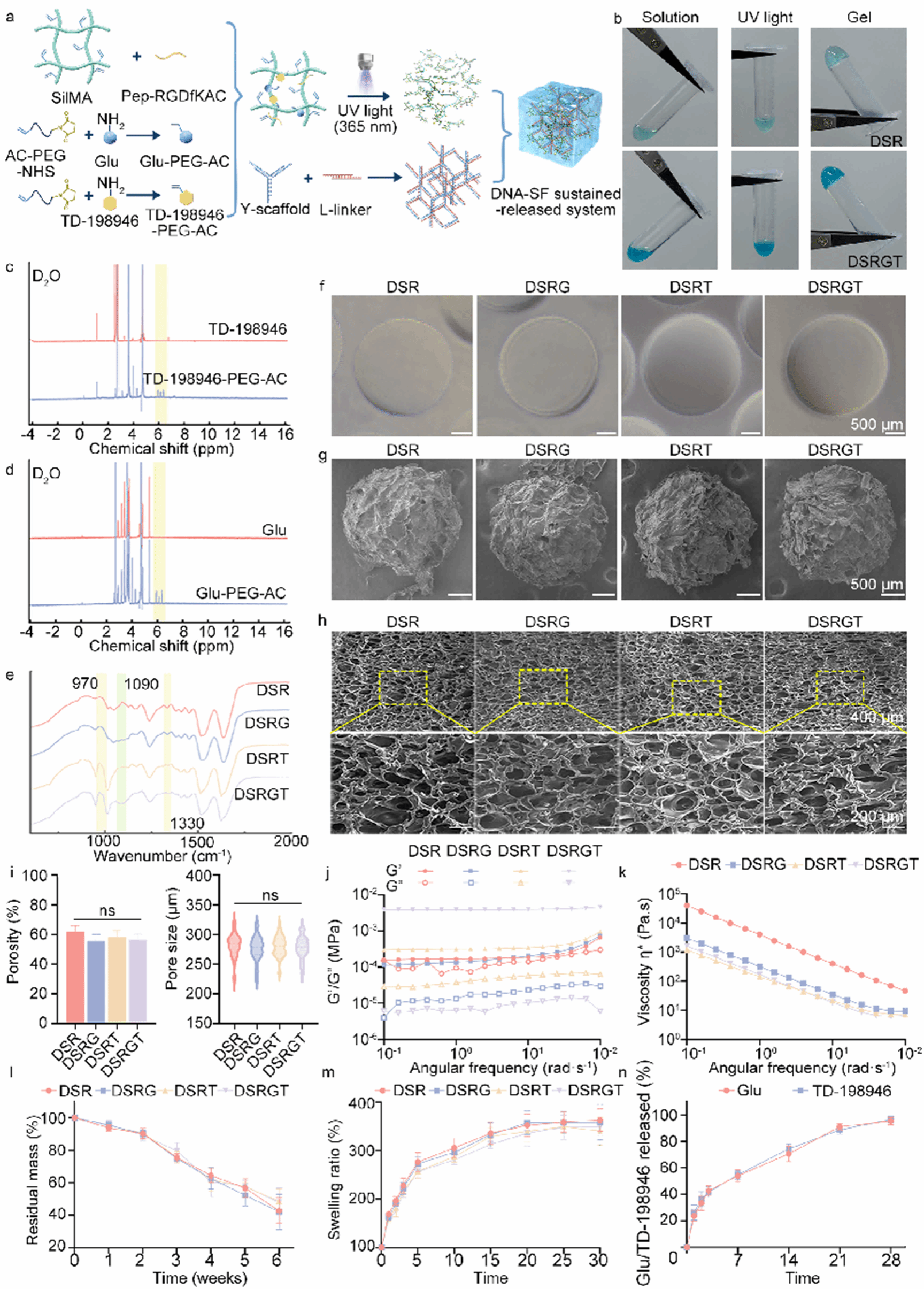
图1. DSRGT的合成与表征。
a. 合成路线与分子相互作用示意;b. 溶胶-凝胶转变;c–d. TD 198946 PEG AC与Glu PEG AC的¹H NMR(D₂O);e. DSR/DSRG/DSRT/DSRGT的FTIR;f. DLP打印球体的宏观图(标尺500 µm);g. 打印球体的FE SEM(500 µm);h. 本体水凝胶FE SEM;i. 孔隙率(n=6)与孔径分布(n=150);j. 储能/损耗模量频扫;k. 黏度 剪切速率曲线;l. 降解曲线(n=6);m. 吸胀比(n=6);n. Glu与TD 198946缓释曲线。
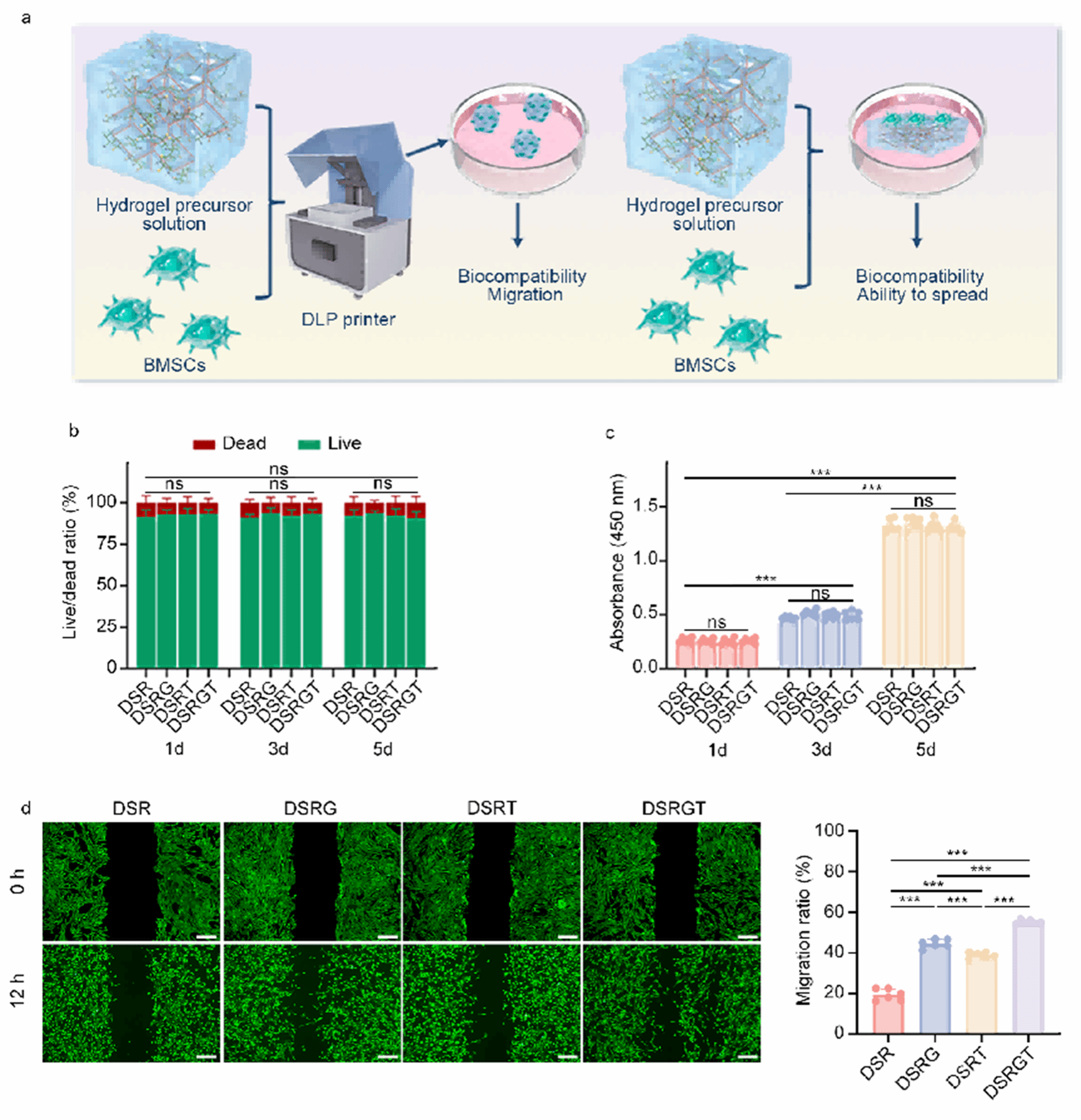
图2. DSR/DSRG/DSRT/DSRGT对BMSCs的相容性与迁移。
a. 设计示意;b. 1/3/5 d活/死染(n=3);c. CCK‑8增殖(n=6);d. 划痕‑定量与Transwell迁移;12 h DSRGT迁移率最高(55.09±1.08%)。
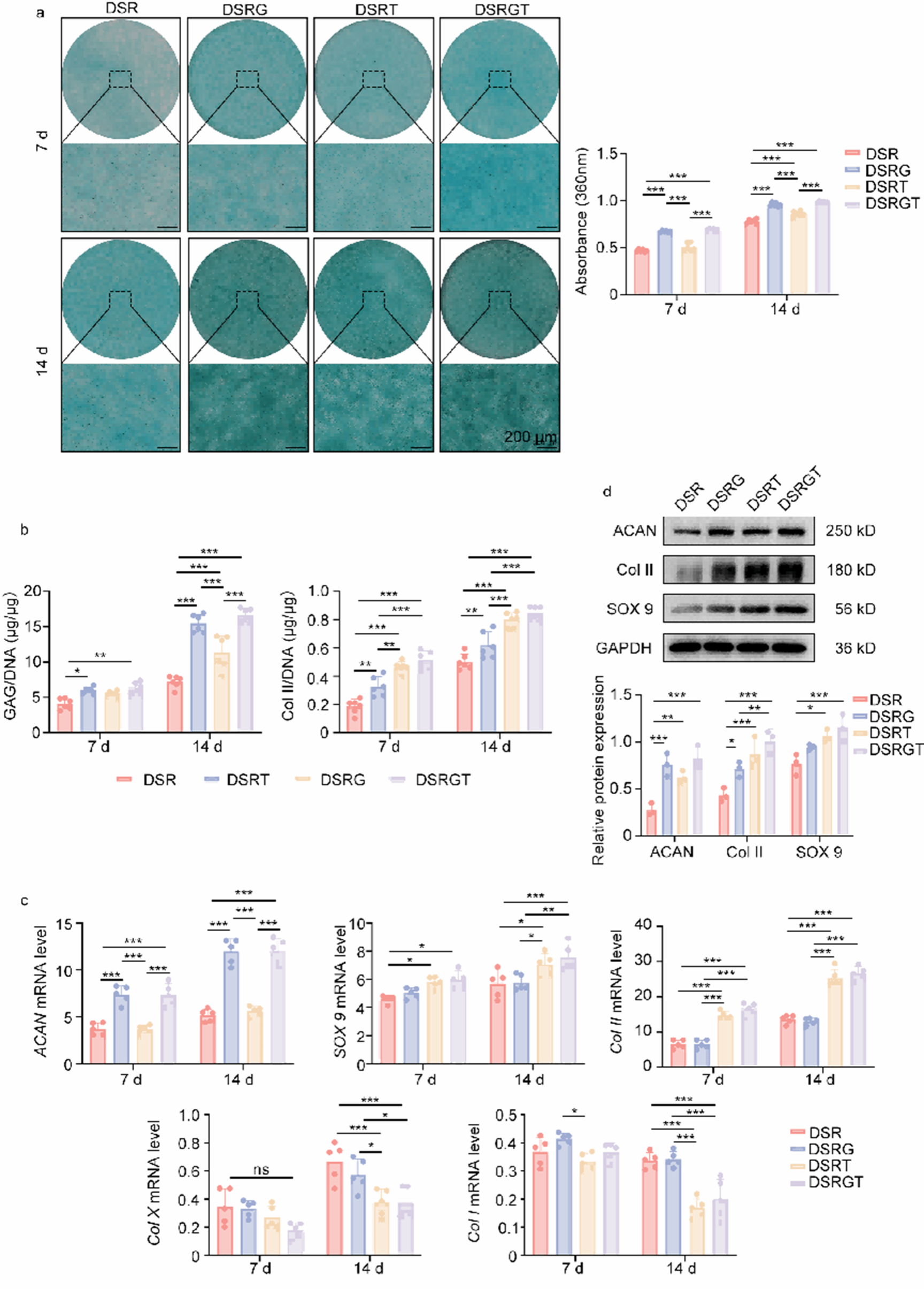
图3. BMSCs的成软骨分化。
a. 7/14 d番红/Alcian blue及定量(n=6);b. GAG与Col II含量(n=6);c. qRT‑PCR(Col I/Col X/ACAN/Col II/SOX9;n=6);d. WB与定量(ACAN/Col II/SOX9;n=3)。DSRGT总体最优。
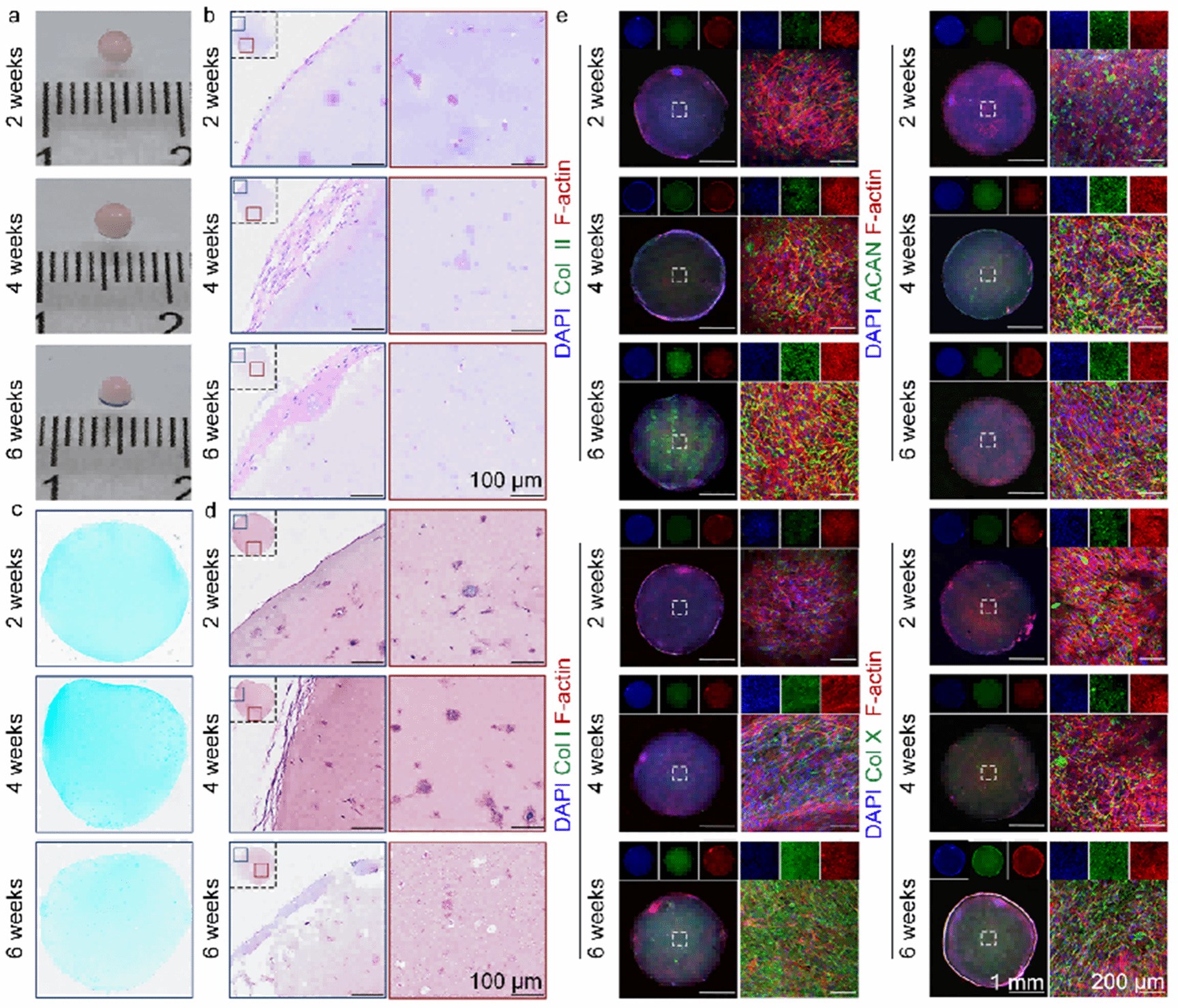
图4. 2/4/6周软骨类器官的结构与标志物。
a. 宏观形态;.b HE;c. Alcian blue;d. SO/FG;e. IF(Col II、ACAN、Col I、Col X;n=6)。4周时GAG与ACAN最强,Col X较低。
通过检测不同培养阶段毫米级软骨类器官的表型,并对其进行mRNA测序分析,进一步明确了软骨类器官在不同时间点的基因表达模式,最终确定4周是软骨类器官向透明软骨分化的最佳培养时间点。
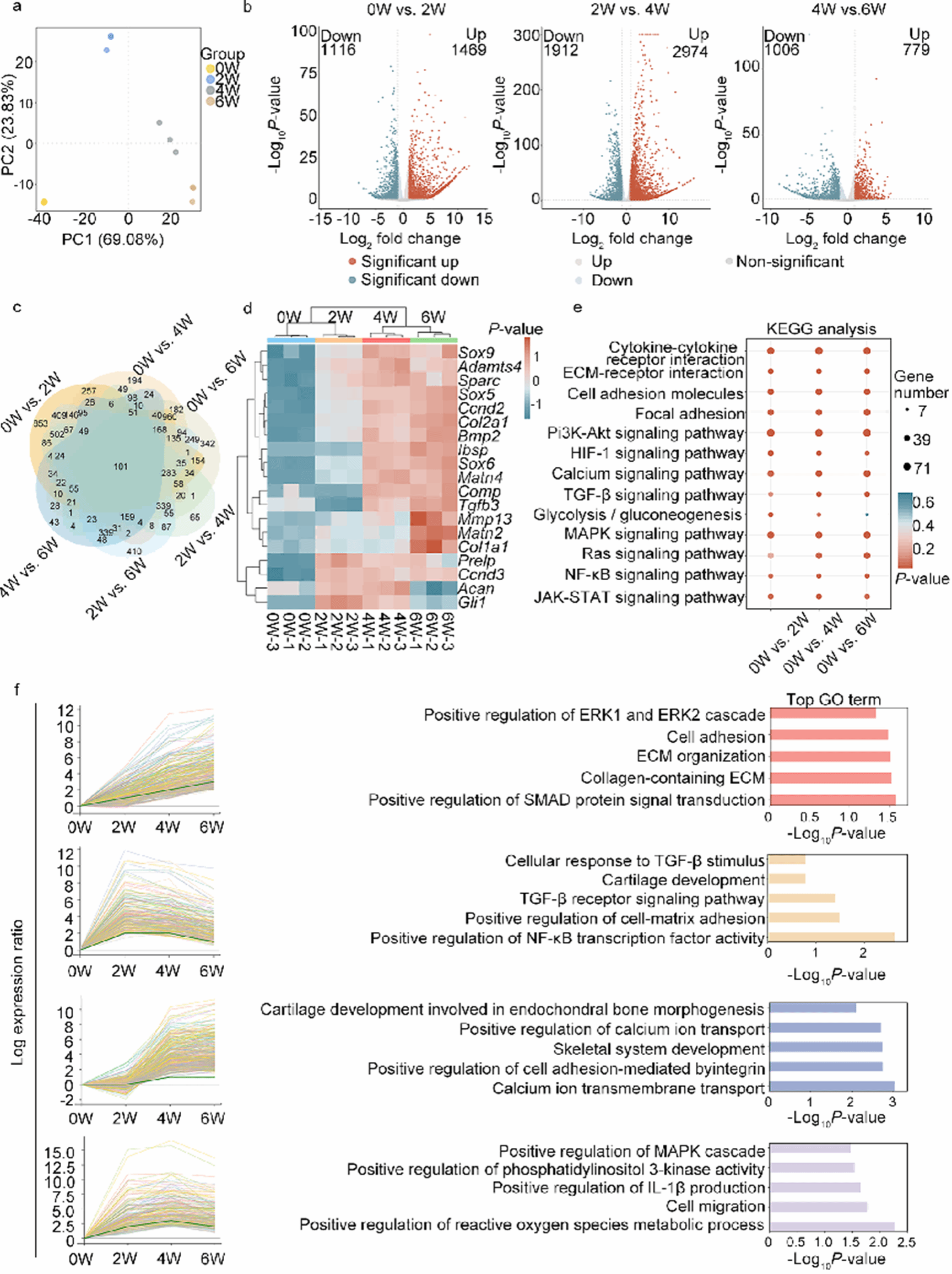
图5. COs在0/2/4/6周的转录组学。
a. PCA(n=3);b. 火山图(0↔2W,2↔4W,4↔6W);c. 维恩图;d. 关键成软骨mRNA热图;e. KEGG富集;f. STEM分析。
随后,将4周培养的软骨类器官移植至大鼠股骨软骨缺损模型中,评估其作为移植物修复软骨缺损的治疗效果。此外,对受损软骨、使用软骨类器官修复8周后的再生软骨以及健康软骨的mRNA进行测序分析,通过体内验证与体外反向验证揭示了由DSRGT构建的软骨类器官通过上调MAPK信号通路促进软骨再生。总之,采用 DSRGT 构建的毫米级软骨类器官为软骨缺损再生提供了一种新颖且有效的策略。
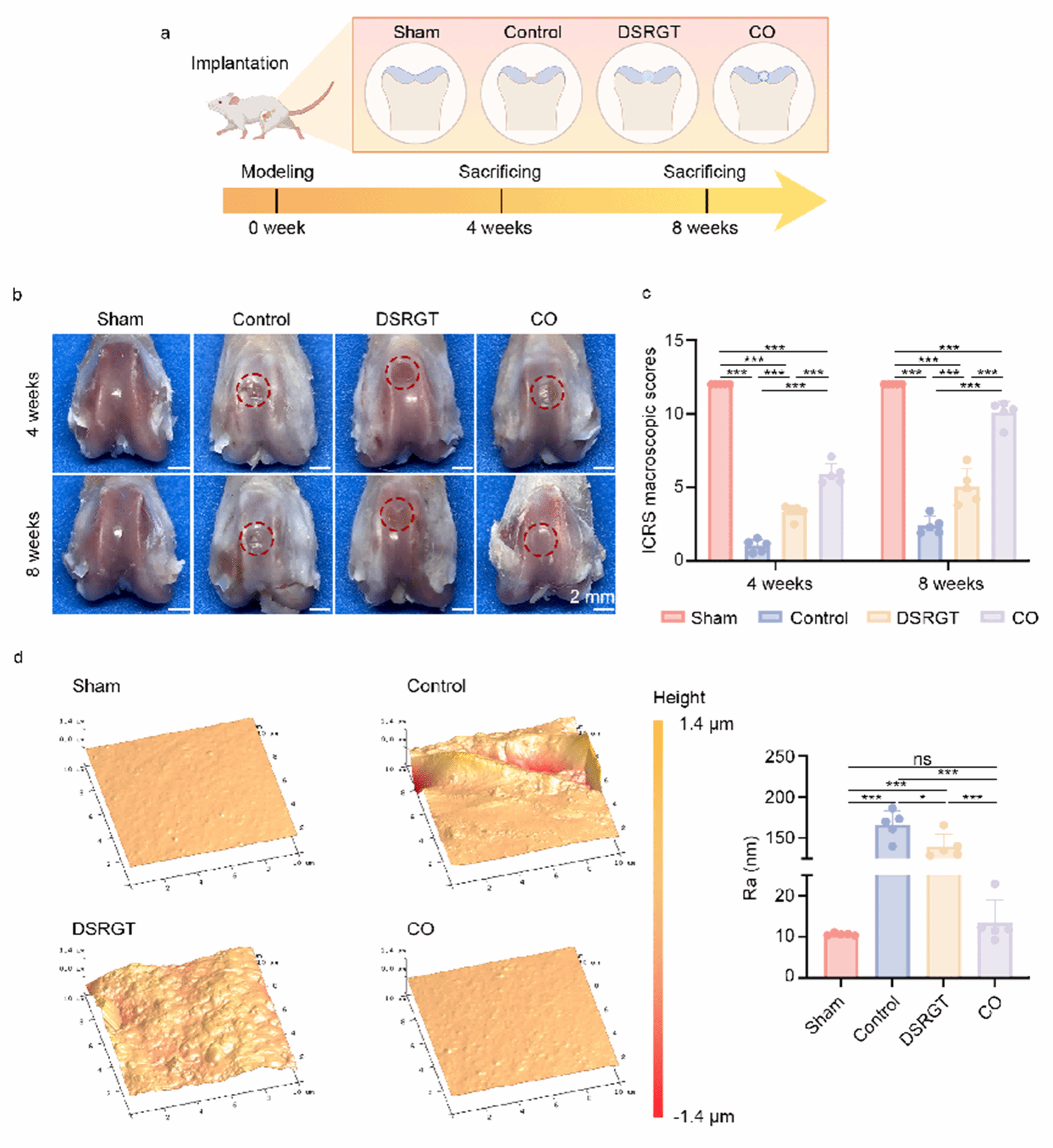
图6 . 体内修复评估。
a. 分组/建模示意;b. 4/8周宏观;c. ICRS评分(n=5):CO组最高;d.AFM粗糙度(8周):CO接近Sham,优于对照与DSRGT。
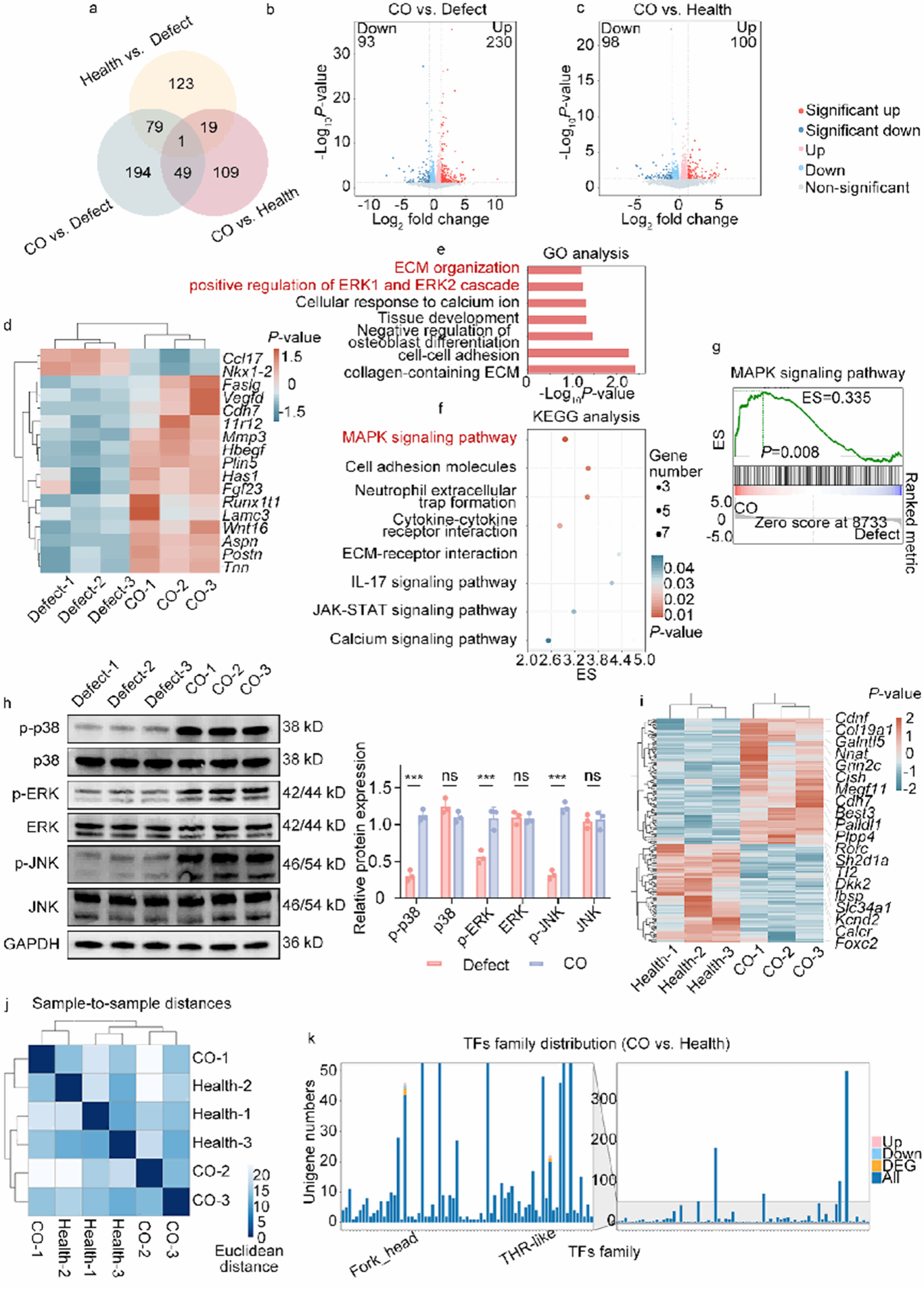
图7. 再生软骨的分子层面接近健康软骨,并上调MAPK。
a. 维恩图;b-c. 火山图(Defect vs CO;CO vs Healthy);d. 再生关键基因热图(Defect vs CO);e. GO;f. KEGG;g. GSEA;h. WB验证(n=3,p p38/p ERK/p JNK↑);i-k CO与Healthy的聚类与TF家族分布。
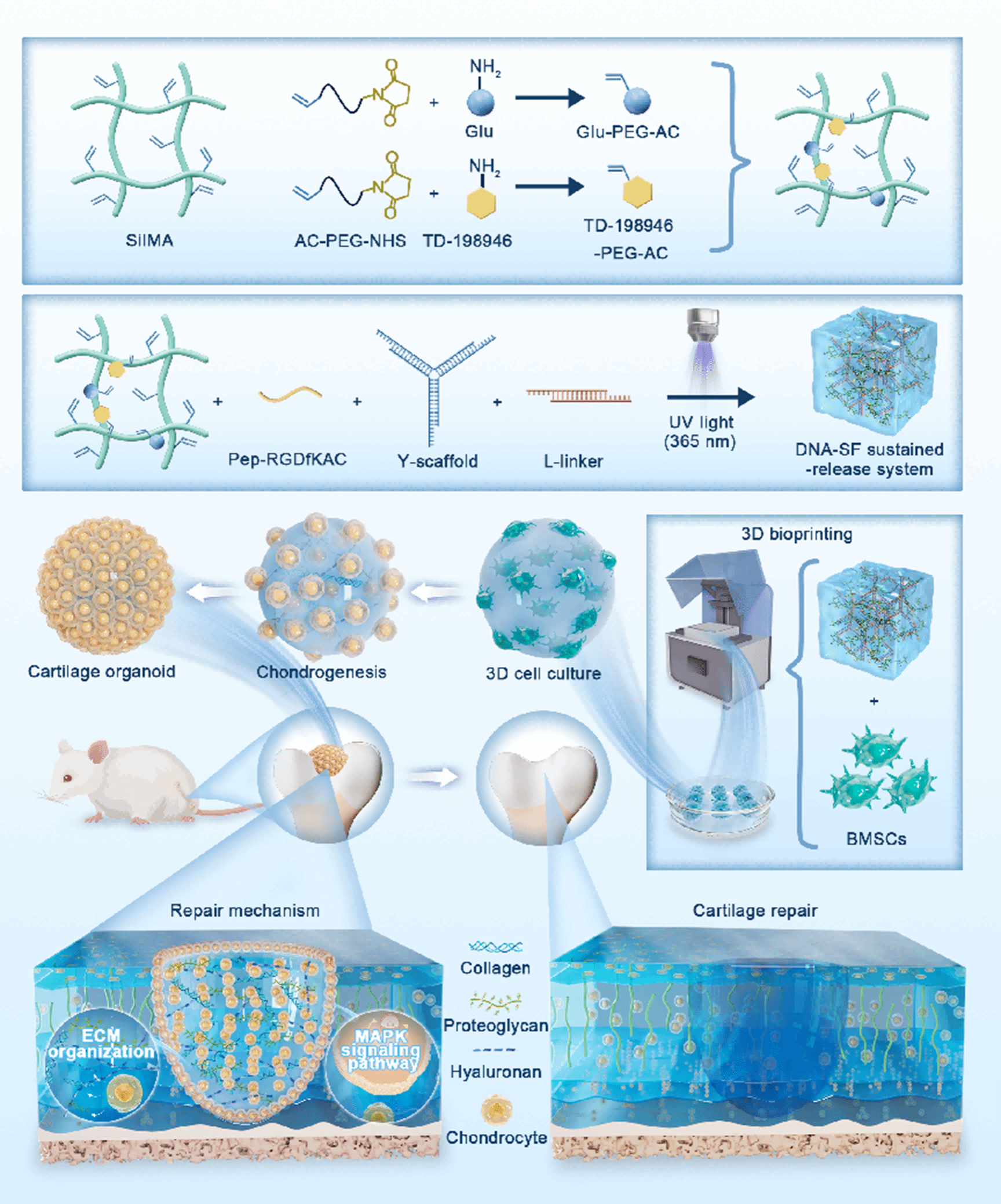
图8. DNA SF缓释系统合成与修复机制示意。
总结与展望
该研究团队此前在多个高水平期刊上发表了6篇综述性文章,系统性总结并深入探讨了为何选择DNA-丝素蛋白(DNA-silk fibroin, DNA-SF)水凝胶作为构建软骨类器官的理想材料(Zhou et al., Theranostics, 2022, 12, 5103–5124;Ma et al., Chemical Engineering Journal, 2023, 477, 147146;Shen et al., Fundamental Research, 2025, 5, 2222-2240;Li et al., Advanced Healthcare Materials, 2024, 13, 2400431;Shen et al., Theranostics, 2025, 15(2), 560–584;Chen et al., Materials Today Bio, 2025, 31, 101509)。在上述理论基础上,研究团队率先成功构建了DNA-SF水凝胶材料(Zhou et al., Materials Horizons, 2024, 11, 1465–1483),并首次利用该水凝胶实现了初代软骨类器官的构建(Shen et al., Bioactive Materials, 2024, 35, 429–444)。在此基础上,团队进一步优化材料性能与组织工程策略,最终实现了基于DNA-SF水凝胶的成熟软骨类器官的构建,标志着该领域的一项重要突破。
文章链接:
https://link.springer.com/article/10.1186/s40779-025-00625-z

