近期,上海大学转化医学研究院苏佳灿教授团队在期刊 Journal of Nanobiotechnology 上发表研究性文章:"Folic acid-modified ginger-derived extracellular vesicles for targeted treatment of rheumatoid arthritis by remodeling immune microenvironment via the PI3K-AKT pathway"。该研究通过差速离心和蔗糖密度梯度离心相结合的方法成功分离了GDEVs,并与FA-PEG2000-Chol相结合制备FA-GDEVs,从而赋予其M1巨噬细胞靶向的能力。通过Zeta电位、透射电子显微镜(TEM)、纳米粒子跟踪分析(NTA)分别对GDEVs和FA-GDEVs的表面电荷、形貌和粒径进行表征,证明此工程化方法不会显著影响GDEVs的形态、尺寸和分散稳定性。高效液相色谱法(HPLC)证实在GDEVs中检测到6-姜辣素和6-姜烯酚。生姜的这些活性成分,以其有效的抗炎特性和多方面的分子靶点而闻名。这一发现提示PEVs可能保留了植物的天然功能,值得进一步探索。上海大学转化医学研究院韩瑞娜硕士研究生、周东阳博士后、纪宁博士研究生、上海中冶医院尹志峰主治医师为论文共同第一作者,上海大学转化医学研究院苏佳灿教授、南通大学附属医院韩庆林主任医师、上海大学转化医学研究院刘晗副研究员、刘心如副研究员为论文共同通讯作者。

研究背景
类风湿关节炎(Rheumatoid arthritis, RA)是一种自身免疫性炎症疾病,以持续性滑膜炎症及后续的关节功能损伤为特征。尽管已有多种传统疗法应用于临床,但这类疗法往往存在显著副作用,且治疗成本高昂。植物源细胞外囊泡(Plant-derived extracellular vesicles, PEVs)因其具备来源丰富、价格低廉、免疫原性低、生物相容性高及可规模化生产等优势,成为极具潜力的替代治疗方案。PEVs可通过转运固有生物活性分子,实现细胞间通讯功能的增强。
文章亮点
材料创新:以天然来源的生姜来源的细胞外囊泡(Ginger-derived extracellular vesicles ,GDEVs)为治疗载体,并对其开展工程化修饰以提升疗效。该方案克服了传统治疗手段的局限性,为疾病治疗提供了一种极具前景的策略。
工程化修饰:基于巨噬细胞表面的叶酸受体对GDEVs进行靶向修饰,实现其在炎症关节部位的高效滞留。该策略借助免疫微环境调控作用,可显著延缓疾病进程,对本领域相关研究具有重要的借鉴意义。
理念创新:首次提出将PEVs应用于RA的治疗方案,再次印证了动植物跨界通讯的全新模式,以及天然物质调控疾病治疗的新机制。该研究不仅为RA乃至其他疾病的治疗提供了全新策略,同时也为PEVs领域的进一步探索提供了研究思路与方向。
该研究通过差速离心和蔗糖密度梯度离心相结合的方法成功分离了GDEVs,并与FA-PEG2000-Chol相结合制备FA-GDEVs,从而赋予其M1巨噬细胞靶向的能力(图1A)。通过Zeta电位、透射电子显微镜(TEM)、纳米粒子跟踪分析(NTA)分别对GDEVs和FA-GDEVs的表面电荷、形貌和粒径进行表征,证明此工程化方法不会显著影响GDEVs的形态、尺寸和分散稳定性(图1B-D)。高效液相色谱法(HPLC)证实在GDEVs中检测到6-姜辣素和6-姜烯酚(图1E)。生姜的这些活性成分,以其有效的抗炎特性和多方面的分子靶点而闻名。这一发现提示PEVs可能保留了植物的天然功能,值得进一步探索。
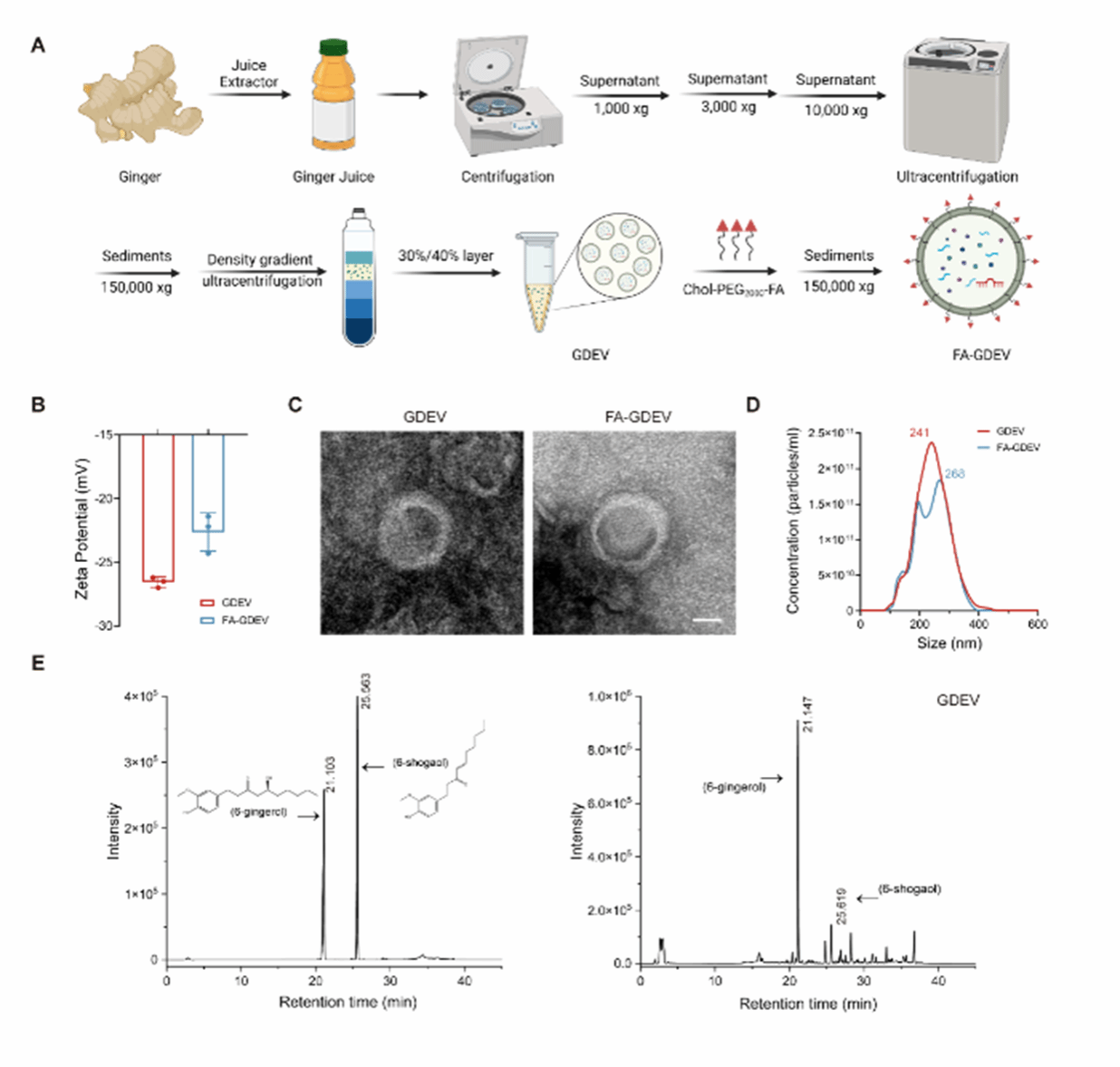
图1
FA修饰使GDEVs对M1巨噬细胞过表达的FR具有特异性结合能力。荧光显微镜和流式细胞术显示,LPS + IFN-γ激活的BMDMs对FA-GDEVs的摄取显著高于未修饰GDEVs。免疫荧光染色确认了FA-GDEVs与FR的高度共定位,证实了FR介导的内吞作用(图2A-C)。在胶原诱导关节炎(CIA)小鼠中,荧光FA-GDEVs显示出更强且更持久的关节荧光信号,特别是在注射后12小时达到峰值,表明其延长了体内循环时间。离体成像和踝关节切片免疫荧光分析进一步证明了FA-GDEVs在炎症关节中的高效积累和FR共定位(图2D-G)。
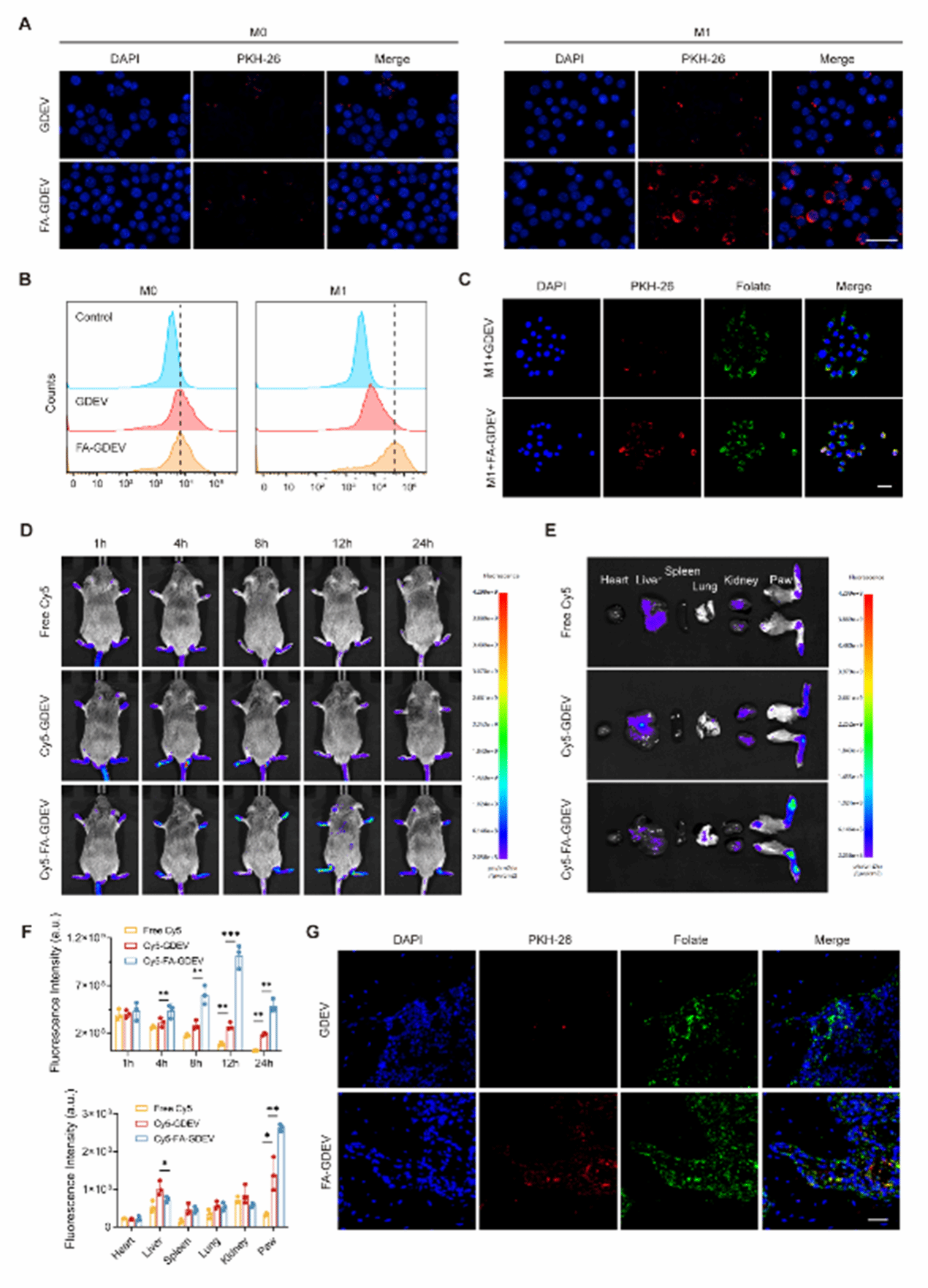
图2
在免疫微环境中,细胞、细胞因子等的互动维持免疫稳态和调节炎症。RA中M1/M2巨噬细胞失衡导致促炎细胞因子过量而抗炎细胞因子减少。调整巨噬细胞极化是转向疾病缓解的关键。作者研究了FA-GDEVs对巨噬细胞极化的影响,通过免疫荧光、流式细胞术、WB和qRT-PCR发现在LPS + IFN-γ刺激后,BMDMs中M1巨噬细胞标记物iNOS表达增加;而FA-GDEVs处理显著降低了iNOS,并增加了M2巨噬细胞标记物CD206的表达,效果优于其他处理组(图3A-E)。模拟炎症滑膜环境的研究进一步证实,FA-GDEVs可减弱iNOS表达并增强CD206表达,展示出强大的免疫调节作用,有效促使巨噬细胞从M1向M2极化,从而减轻炎症反应(图3F)。
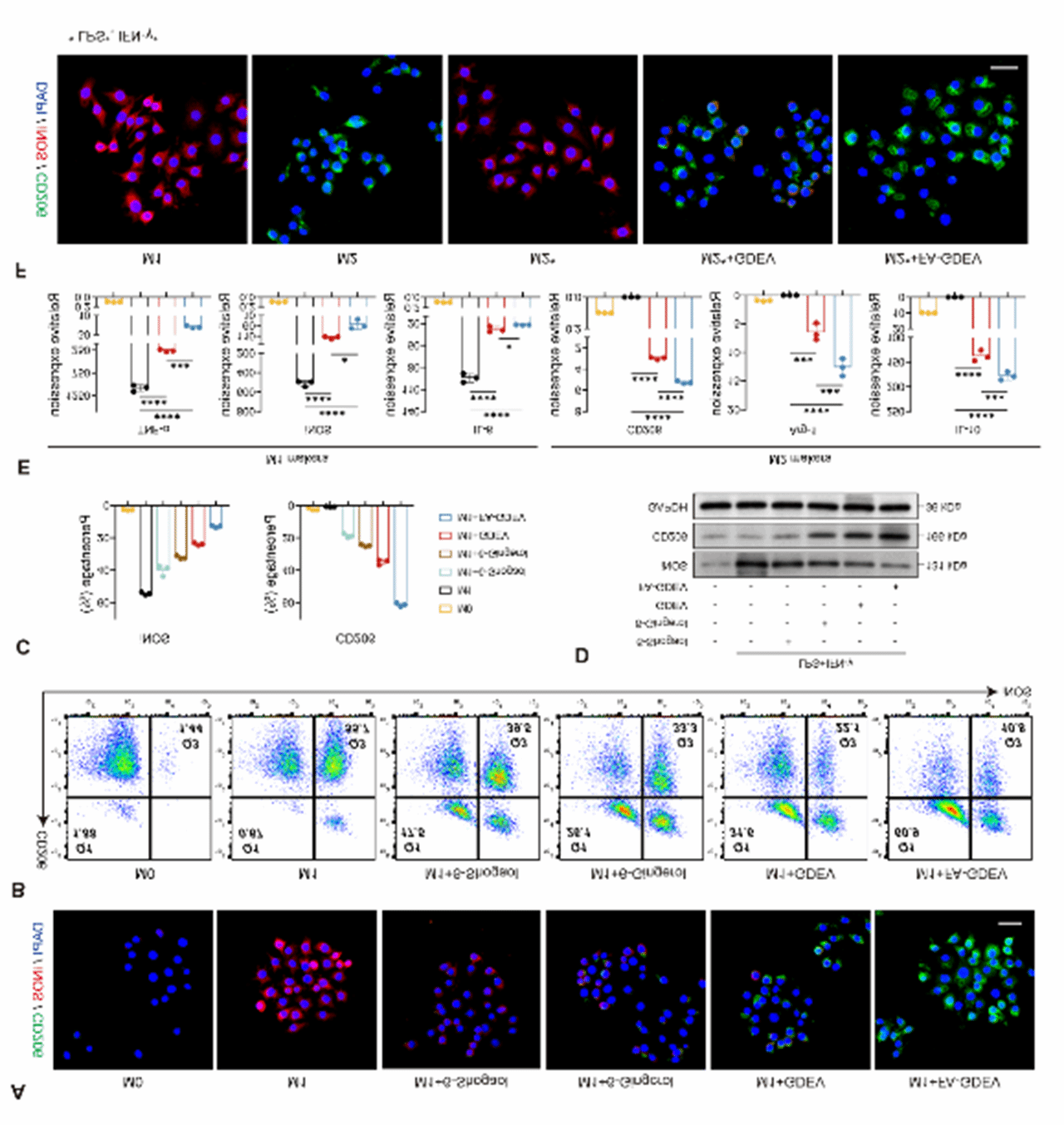
图3
EVs通过转移内源性miRNAs促进细胞间通讯调节基因表达。作者对GDEVs和FA-GDEVs进行了miRNA测序,发现前20个高表达miRNAs在两者间无显著差异,且富含姜来源的miRNAs,表明PEVs可递送活性植物核酸至哺乳动物细胞。进一步研究显示,FA-GDEVs中的人类miRNAs如has-miR-22-3p、has-miR-143-3p等参与了炎症疾病的免疫反应调控。GO分析揭示这些miRNAs与蛋白自磷酸化、转录调控等功能相关;KEGG分析表明它们参与PI3K-Akt通路,影响巨噬细胞M1到M2极化(图4A-B)。为了验证FA-GDEVs的作用机制,使用WB检测到其处理后PI3K和AKT磷酸化水平增加,伴随iNOS和CD206表达提升。加入PI3K-AKT抑制剂LY294002后,FA-GDEVs的效果消失,免疫荧光染色结果一致(图4C-E)。
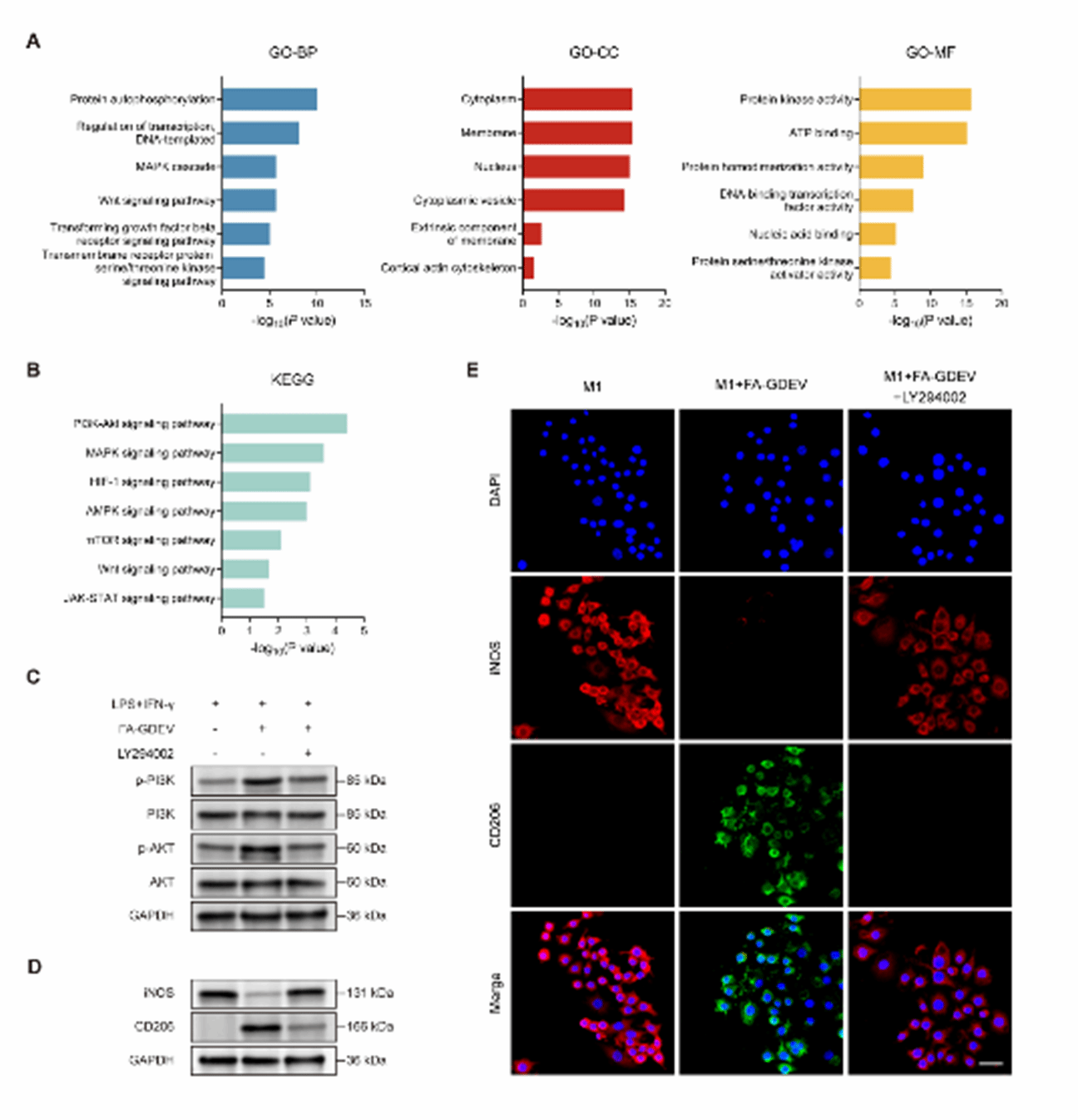
图4
作者评估了FA-GDEVs在CIA小鼠模型中的疗效,使用甲氨蝶呤(MTX)作为阳性对照。治疗结束时的照片显示,FA-GDEVs显著缓解RA症状,优于GDEVs和MTX(图5B)。组织学检查发现,CIA组有明显炎症细胞浸润、滑膜炎和软骨退化;而FA-GDEVs组病理改变最小,接近野生型水平(图5C)。临床评估表明,FA-GDEVs治疗的小鼠关节炎症和足跖水肿最轻,疾病进展减缓(图5D-E)。脾脏和胸腺指数分析显示,FA-GDEVs和MTX组与野生型相似(图5F)。FA-GDEVs显著降低了促炎细胞因子TNF-α、IL-6和IL-1β的水平,并减少了破骨细胞计数,促进骨修复(图5G-H)。micro-CT成像证实,FA-GDEVs改善了骨侵蚀,恢复了BV/TV、Tb和BS/BV比率至正常水平(图5I-J)。免疫荧光染色显示,FA-GDEVs显著降低M1巨噬细胞水平,增强M2巨噬细胞水平(图5K)。
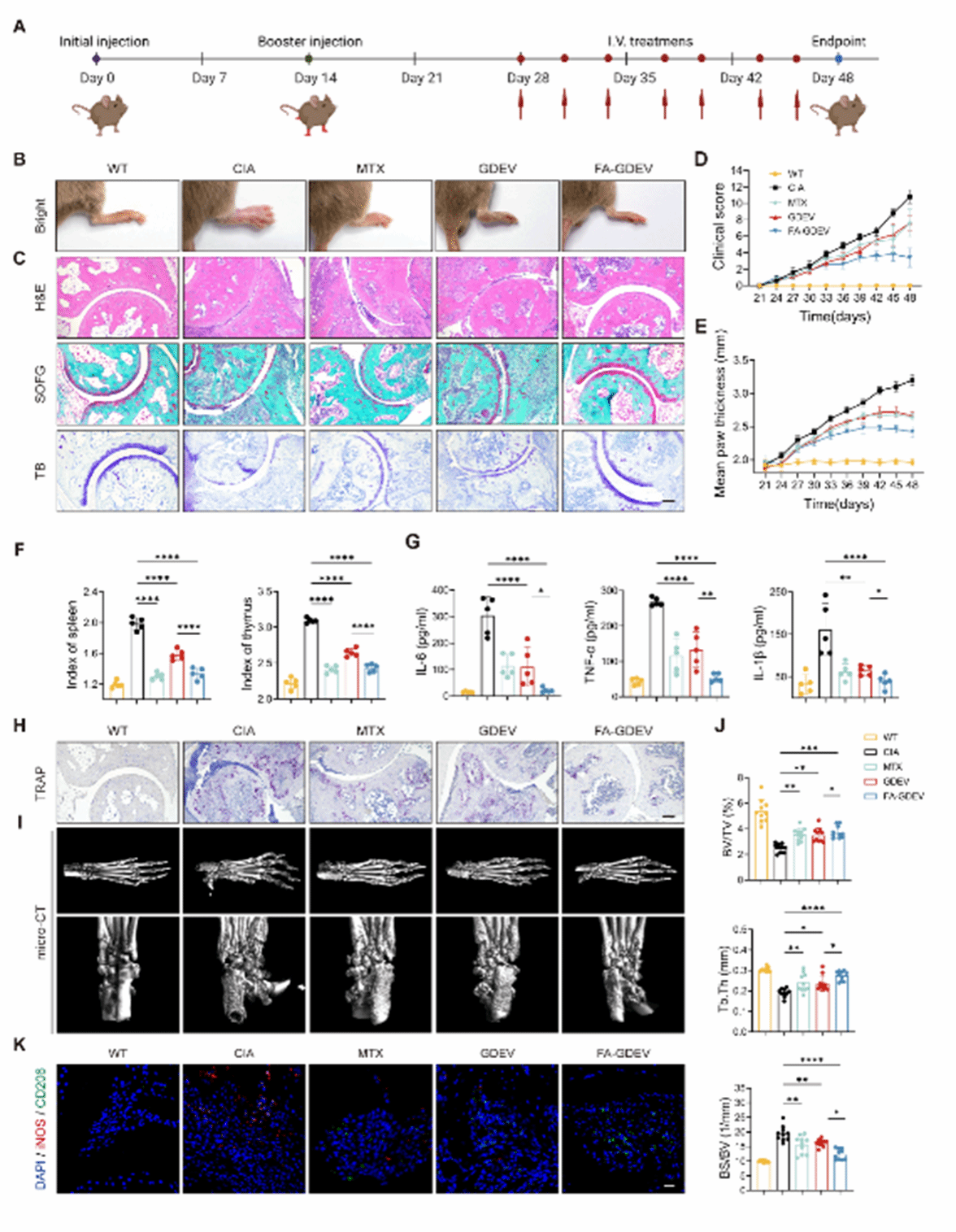
图5
最后,本研究通过H&E染色评估了FA-GDEVs对小鼠主要器官的影响,未发现明显毒性或组织损伤(图6A)。此外,FA-GDEVs静脉给药无溶血作用,并能有效减轻RA相关的体重下降(图6B-C)。
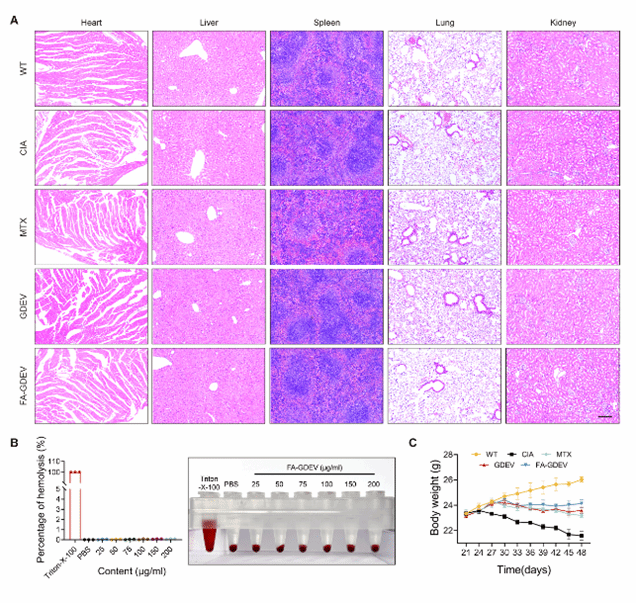
图6
总结与展望
苏佳灿教授团队在EVs领域具有丰富的研究经验,已经发表了多篇细胞外囊泡相关的高水平论文,包括MEVs,BEVs、PEVs和OEVs等。此前,苏佳灿教授团队在Nano Research上发表了题为“Engineered plant extracellular vesicles for autoimmune diseases therapy”的综述文章(2024年度封面文章),系统介绍了PEVs的生物发生、理化和生物学特性、内化机制、分离方法及其在各种疾病中的应用,并特别关注其在AID中的潜在作用,全面总结了PEVs的工程化方法和给药途径,展望了利用PEVs在AID治疗中的优势和挑战,此工作奠定了夯实的基础。
该研究通过开发针对活化巨噬细胞的GDEVs(即FA-GDEVs),引入了一种治疗RA的创新方法。作为强效的天然免疫调节剂,FA-GDEVs在CIA小鼠模型中显示出显著缓解RA症状的能力。这种有益效果归因于通过 PI3K-AKT通路调节了M1巨噬细胞的极化,从而促进了向M2巨噬细胞表型的转变。该研究首次阐明了利用GDEVs治疗RA的功能机制。这种调控机制可能超越RA的范围,涵盖一系列以巨噬细胞参与为特征的疾病。FA-GDEVs能够作为一类新型生物活性药物出现,凸显了植物疗法在调节免疫反应方面的新兴意义。这为前瞻性研究和临床应用提供了一个良好的途径。

