近期,上海大学转化医学研究院苏佳灿教授团队在期刊 Advanced Materials 上发表研究性文章:"High-Efficiency Targeted Mitochondrial Transfer and AUTAC4-Enhanced Dual Renewal Strategy for Rheumatoid Arthritis"。本研究针对类风湿关节炎(RA)治疗中常规生物材料靶向性差及无法逆转线粒体损伤的瓶颈,开发一种名为“双重作用线粒体更新疗法”(DAMRT)的仿生递送系统。该系统利用叶酸修饰的巨噬细胞膜伪装,实现对病灶部位活化M1型巨噬细胞的精准靶向,并通过负载自噬靶向嵌合体(AUTAC4)特异性清除受损线粒体,同时引入健康的间充质干细胞(MSC)线粒体以恢复能量代谢,从而通过抑制铁死亡途径有效促使促炎M1巨噬细胞向抗炎M2表型重编程。在体内实验中,DAMRT显著减轻关节炎小鼠的滑膜炎症、软骨降解及骨质破坏,且具备良好的生物安全性。展望未来,该策略不仅确立利用“活体材料”恢复细胞稳态的通用治疗平台,有望扩展至其他线粒体功能障碍疾病及骨类器官的能量供应模块,后续研究若结合微流控技术优化制备工艺,将进一步推动其在再生医学领域的标准化与临床转化。上海大学转化医学研究院汪拂晓博士后、上海交通大学医学院附属新华医院张浩主治医师、上海大学转化医学研究院周东阳博士后、唐璇博士研究生为论文共同第一作者,上海大学转化医学研究院苏佳灿教授、白龙副研究员、上海交通大学医学院附属新华医院胡衍主治医师、上海大学转化医学研究院徐可研究员为论文共同通讯作者。

研究背景
类风湿性关节炎(RA)是一种全球范围内高发的慢性自身免疫性疾病,患者数量约达数千万,具有高致残率和较高死亡风险,对人类健康造成长期威胁。尽管近年来生物材料递送系统(如纳米颗粒、脂质体及高分子微球等)被广泛用于将抗炎药物或活性分子靶向输送至病变关节,但其在临床应用中仍面临靶向精度不足、递送效率低、生物相容性有限及体内代谢稳定性差等关键瓶颈,难以有效应对RA复杂的炎症微环境。研究表明,巨噬细胞在RA慢性炎症进程中发挥核心调控作用,其中促炎型M1巨噬细胞主导炎症反应,而抗炎型M2巨噬细胞则参与组织修复与再生。尤其是M1巨噬细胞中线粒体功能障碍可诱导活性氧积累并加剧炎症,同时抑制其向M2表型转化,因此恢复线粒体稳态、调控能量代谢被认为是干预RA的重要策略。然而,传统药物难以逆转病理状态下线粒体结构与功能的不可逆损伤。近年来,“活性材料”理念的提出为疾病治疗提供新思路,其中线粒体作为具有生物活性的细胞器,能够在细胞间转移并重建受体细胞的能量代谢与稳态调控,这种独特的动态适应能力使其在RA治疗中展现出重要潜力与研究价值。
本文亮点
首创“双重线粒体更新”策略,协同实现受损清除与健康补充:该研究提出一种名为DAMRT的双重作用疗法,通过整合自噬靶向嵌合体(AUTAC4)与外源性健康线粒体,实现对细胞内环境的全面重塑。该策略一方面利用AUTAC4特异性诱导内源性受损、片段化线粒体的自噬清除,另一方面通过移植间充质干细胞(MSC)来源的健康线粒体恢复细胞生物能量,从而彻底恢复线粒体稳态。
2.构建叶酸修饰的仿生靶向递送系统,显著突破线粒体转运效率瓶颈:研究团队设计一种叶酸修饰的巨噬细胞膜伪装载体,使其能够精准靶向类风湿关节炎(RA)关节中活化的M1型巨噬细胞,并实现免疫逃逸。这种仿生工程化设计有效解决传统线粒体疗法依赖被动内吞、靶向性差的难题,将线粒体的胞内递送效率提高两倍以上,确保治疗物质在病灶部位的高效富集。
3.抑制铁死亡并重塑巨噬细胞极化,在RA模型中展现卓越治疗效能:机制研究表明,DAMRT能够通过上调Gpx4并下调Acsl4和Tfrc表达来有效抑制巨噬细胞的铁死亡,同时促进促炎M1型巨噬细胞向抗炎M2型表型转化。在胶原诱导的关节炎(CIA)小鼠模型中,该疗法显著减轻滑膜炎症,缓解软骨降解和骨破坏,为治疗RA及其他线粒体功能障碍相关疾病提供新的通用平台。
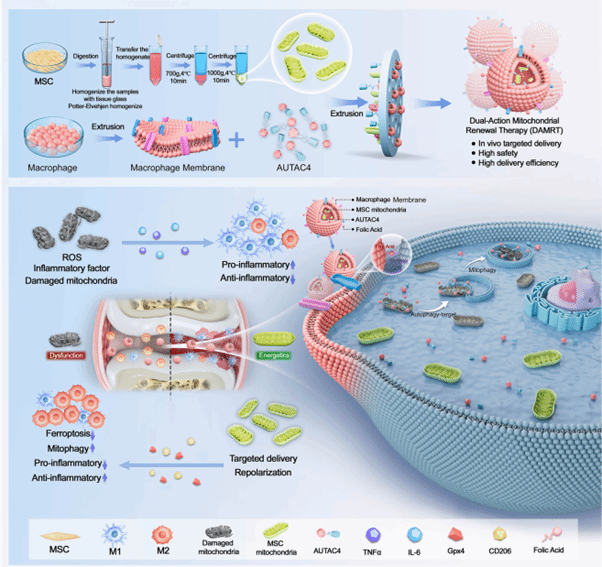
图1:DAMRT的构建及其治疗RA的应用示意图
图解:巨噬细胞膜提取物与分离的间充质干细胞(MSC)线粒体及AUTAC4混合形成DAMRT。CIA小鼠模型中DAMRT治疗的示意图,以及DAMRT对线粒体的调节及其在RA中的应用。AUTAC4促进巨噬细胞中的线粒体自噬,从而清除受损的线粒体。
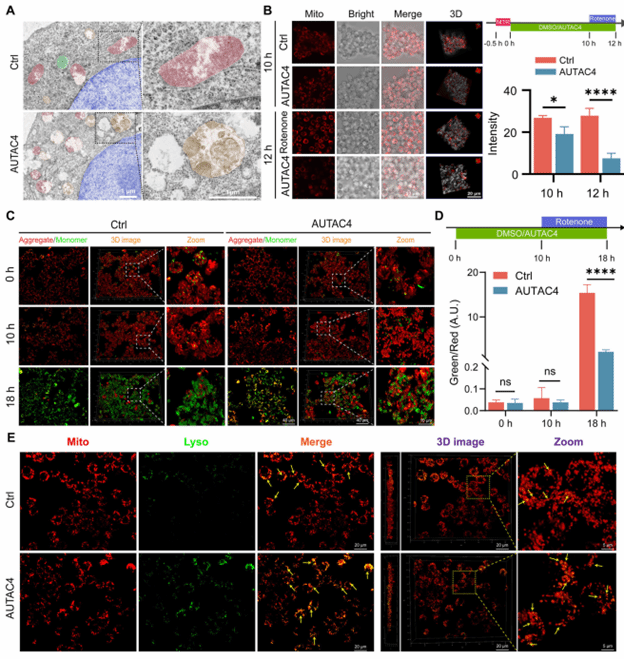
图2:AUTAC4促进巨噬细胞线粒体自噬的验证
图解:(A) 线粒体自噬的代表性透射电镜(TEM)图像,对照组接受鱼藤酮以诱导线粒体损伤,AUTAC4组接受相同的鱼藤酮处理随后进行AUTAC4处理,图中绿色代表线粒体,红色代表功能障碍线粒体,黄色代表线粒体自噬;(B) 用MTR标记线粒体后,用AUTAC4处理巨噬细胞,并在处理后期用鱼藤酮诱导线粒体损伤,通过共聚焦显微镜评估线粒体动力学;(C) JC-1染色测定显示AUTAC4恢复鱼藤酮诱导的巨噬细胞的线粒体膜电位,实验中在AUTAC4处理开始后加入鱼藤酮以诱导功能障碍;(D) JC-1染色的统计定量分析;(E) 线粒体和溶酶体的共定位观察。
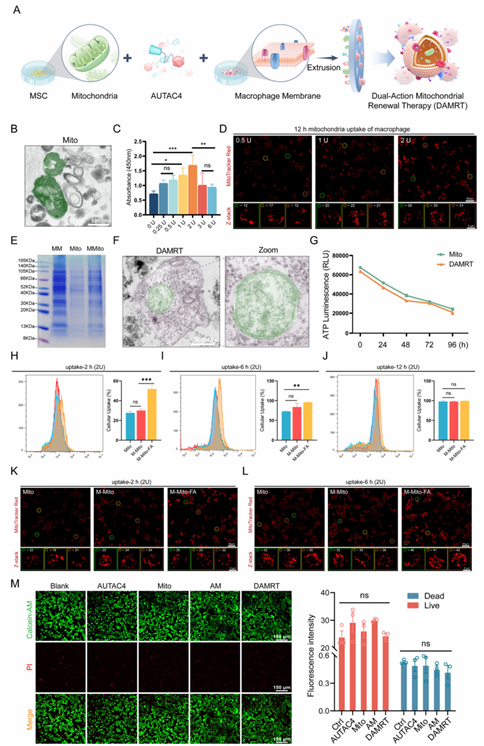
图3:DAMRT的制备与表征
图解: (A) 构建DAMRT的过程示意图,包括MSC来源线粒体的提取、巨噬细胞膜制备和AUTAC4的掺入;(B) 显示提取的完整MSC线粒体的TEM图像,表明其结构完整性;(C) CCK-8检测评估不同线粒体浓度对巨噬细胞增殖的影响;(D) 共聚焦显微镜图像显示不同线粒体浓度下巨噬细胞对线粒体的摄取;(E) 蛋白图谱的SDS-PAGE分析;(F) DAMRT的代表性TEM图像;(G) 在体外不同时间点对Mito和DAMRT组进行ATP活性测量;(H-J) 流式细胞术分析M-Mito-FA、Mito和M-Mito处理不同时间后M1型巨噬细胞的线粒体摄取情况;(K, L) 巨噬细胞在2小时(K)和6小时(L)摄取线粒体的共聚焦显微镜图像;(M) 使用PI和Calcein AM染色评估各种处理后的细胞活力,并对各处理后的活细胞和死细胞进行定量分析。
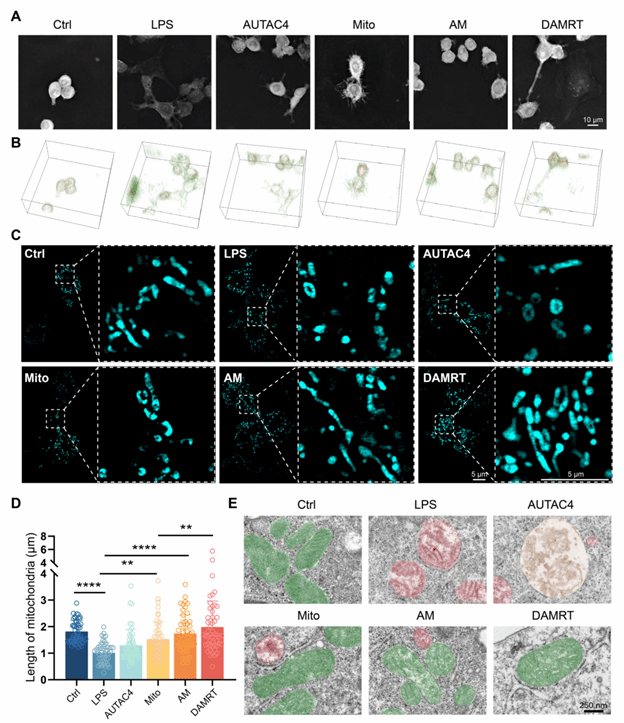
图4:体外巨噬细胞线粒体的形态学观察
图解: (A) 处理后24小时不同组别的代表性Nanolive图像,展示细胞结构;(B) Nanolive的3D透视图,其中细胞膜显示为绿色,线粒体显示为橙色;(C) 记录标记有PKMDR的线粒体嵴的代表性HIS-SIM图像;(D) HIS-SIM结果的定量分析;(E) 线粒体和线粒体自噬的代表性TEM图像,其中绿色代表线粒体,红色代表功能障碍线粒体,黄色代表线粒体自噬 。
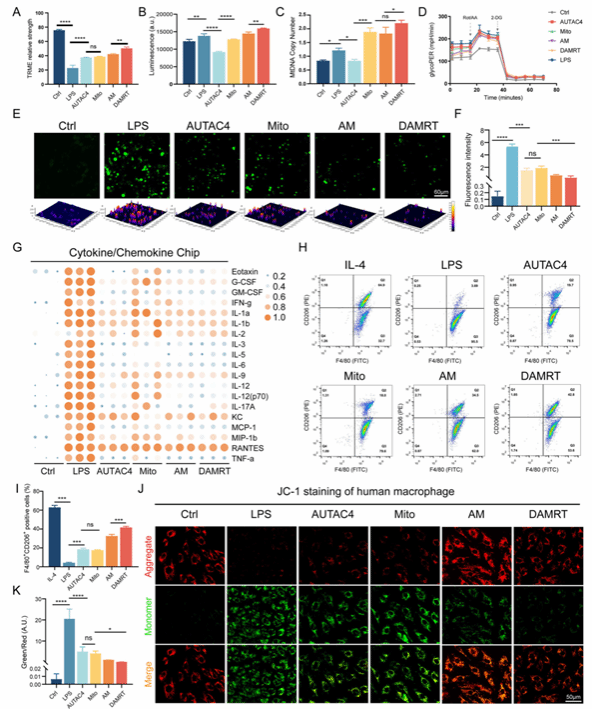
图5:体外巨噬细胞的线粒体调节和免疫调节
图解:实验使用LPS诱导M1型巨噬细胞极化,随后用各实验组(AUTAC4, Mito, AM, DAMRT)进行处理。(A) 评估线粒体膜电位的流式细胞术分析;(B) 细胞内线粒体ATP生成的分光光度法测量;(C) mtDNA定量为线粒体基因拷贝数的比率;(D) 巨噬细胞用LPS预处理以诱导炎症状态,随后用各实验组再处理,使用Seahorse XF糖酵解速率测定法测量糖酵解速率,并随时间监测glycoPER;(E) 处理后通过DCFDA染色测量细胞内ROS;(F) 使用荧光法对ROS产生强度进行定量分析;(G) 基于Luminex的多重检测显示的所研究细胞因子的浓度;(H) 流式细胞术测量M2型巨噬细胞标志物CD206的表达;(I) 图5H中流式细胞术结果的定量分析;(J) 人骨髓来源的巨噬细胞用LPS处理后,用各组药物干预,使用JC-1测定评估线粒体膜电位,绿/红荧光比率指示线粒体膜去极化的程度;(K) JC-1测定的定量分析。
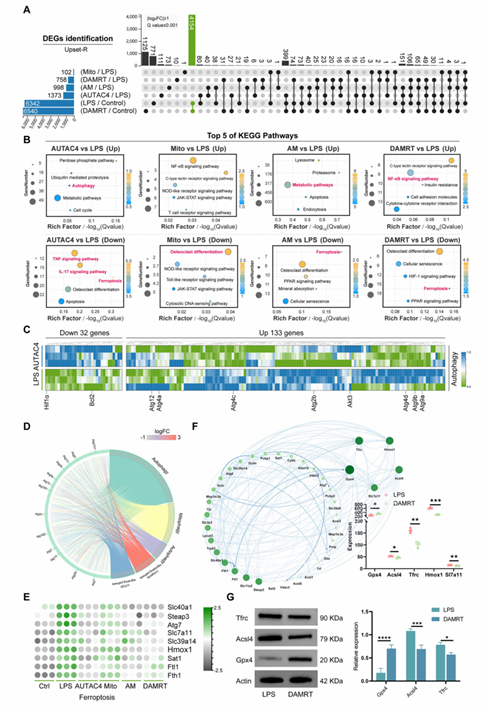
图6:巨噬细胞中的RNA-seq验证
图解:(A) 鉴定DEGs以确定所有可能组合模式下的差异基因集;(B) AUTAC4 vs LPS、Mito vs LPS、AM vs LPS和DAMRT vs LPS的前5个通路富集分析;(C) AUTAC4 vs LPS差异表达的自噬相关基因的热图;(D) 差异表达的自噬相关基因的KEGG富集分析的圆形可视化图;(E) 差异表达的铁死亡相关基因的热图,颜色标尺表示铁死亡相关基因表达值逐渐增加;(F) DAMRT vs LPS的蛋白相互作用分析,右侧集合显示每次比较中关键介质的详细表达谱;(G) LPS和DAMRT组中铁死亡相关蛋白(Gpx4, Acsl4和Tfrc)的Western blot分析。
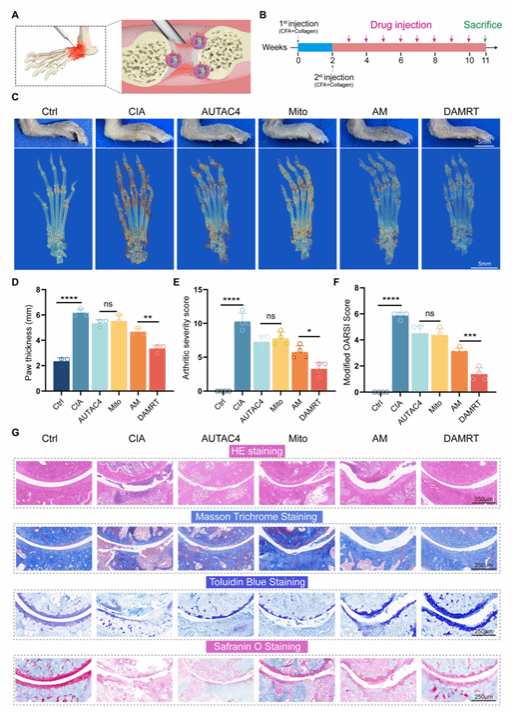
图7:CIA模型小鼠关节炎关节的组织学评估
图解:(A) DAMRT的注射策略;(B) CIA模型建立方案;(C) CIA小鼠模型的爪子代表性图像及后爪Micro-CT成像,对照组接受PBS注射,骨赘定义为超出原始皮质骨轮廓的矿化突起,在3D重建图像中通过不同颜色(橙色)识别;(D) 第一次注射后第11周的爪厚度评估;(E) 第一次注射后第11周的爪肿胀评分评估;(F) 显微镜观察软骨的改良OARSI评分;(G) 小鼠踝关节的H&E染色、Masson三色染色、甲苯胺蓝染色和番红-O染色 。
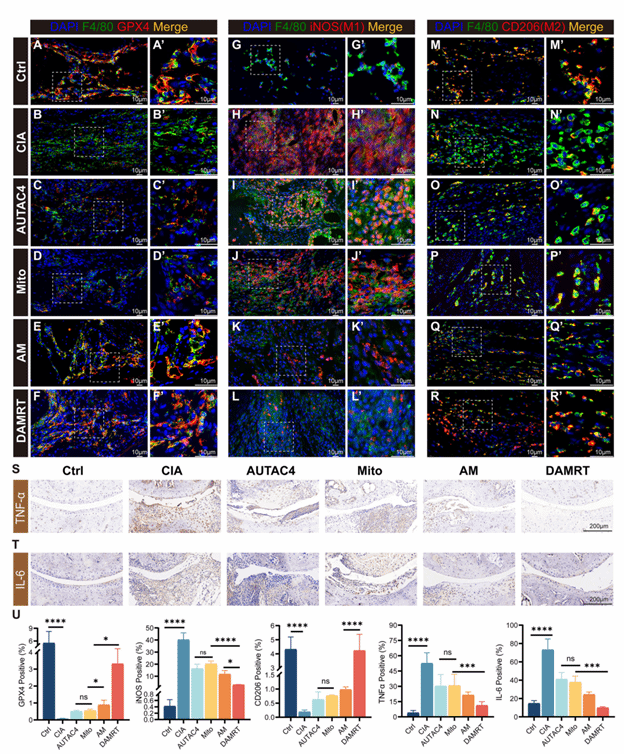
图8:DAMRT通过铁死亡对CIA免疫和炎症的影响
图解:(A-F) 用各种材料处理的踝关节中Gpx4+和F4/80+巨噬细胞的免疫荧光图像,A'-F'是A-F中方框区域的高倍放大图像;(G-L) 用各种材料处理的踝关节中iNOS+和F4/80+巨噬细胞的免疫荧光图像,G'-L'是G-L中方框区域的高倍放大图像;(M-R) 用各种材料处理的踝关节中CD206+和F4/80+巨噬细胞的免疫荧光图像,M'-R'是M-R中方框区域的高倍放大图像;(S-T) 用各种材料处理的踝关节中炎症因子TNF-a (S) 和 IL-6 (T) 的免疫组化图像;(U) 基于免疫荧光和免疫组化结果,定量分析不同样品处理的踝关节组织中Gpx4+、iNOS+、CD206+、TNF-a和IL-6的产生。
总结与展望
本研究针对类风湿关节炎(RA)治疗中常规生物材料靶向性差及无法逆转线粒体损伤的瓶颈,开发一种名为“双重作用线粒体更新疗法”(DAMRT)的仿生递送系统。该系统利用叶酸修饰的巨噬细胞膜伪装,实现对病灶部位活化M1型巨噬细胞的精准靶向,并通过负载自噬靶向嵌合体(AUTAC4)特异性清除受损线粒体,同时引入健康的间充质干细胞(MSC)线粒体以恢复能量代谢,从而通过抑制铁死亡途径有效促使促炎M1巨噬细胞向抗炎M2表型重编程。在体内实验中,DAMRT显著减轻关节炎小鼠的滑膜炎症、软骨降解及骨质破坏,且具备良好的生物安全性。展望未来,该策略不仅确立利用“活体材料”恢复细胞稳态的通用治疗平台,有望扩展至其他线粒体功能障碍疾病及骨类器官的能量供应模块,后续研究若结合微流控技术优化制备工艺,将进一步推动其在再生医学领域的标准化与临床转化。

