近日,Organoid research期刊在线发表香港中文大学李中教授团队最新综述《Bioengineered Materials-driven Construction of Musculoskeletal Organoids for Modeling Aging: Strategies, Applications and Future Perspectives》。该文章系统阐述如何利用生物材料构建肌肉骨骼类器官,以模拟衰老过程。文章重点总结当前构建衰老肌肉骨骼类器官的策略,明确通过材料设计再现衰老微环境的关键原则,并提出一个将材料参数与肌肉骨骼衰老标志、功能验证实验相整合的创新框架。该综述为在体外可控、可调地模拟人体肌肉骨骼系统衰老提供重要的理论依据与技术路径,有望推动衰老机制研究、药物筛选及再生医学治疗的进展。
文章信息
题目:Bioengineered Materials-driven Construction of Musculoskeletal Organoids for Modeling Aging: Strategies, Applications and Future Perspectives
作者:Qiongjiao Zeng, Denghui Xie, Di Wang, Chao Zheng, Liu Yang, Mario Rothbauer, Yiting Lei*, Zhong Alan Li*
引用信息:Qiongjiao Zeng, Denghui Xie, Di Wang, et al. Bioengineered materials-driven construction of musculoskeletal organoids in aging research: Strategies, applications, and future perspectives. Organoid Res, 2025, 1(4), 025450033. https://doi.org/10.36922/OR025450033
文章链接:
https://accscience.com/journal/OR/1/4/10.36922/OR025450033
文章简介
年龄相关性肌肉骨骼系统退变是导致老年群体运动功能丧失、生活质量下降及医疗负担上升的核心驱动因素,其分子调控机制与靶向干预研究长期受限于缺乏精准复刻人类生理病理特征的实验模型。传统二维培养与动物模型均存在显著局限;肌肉骨骼类器官虽能凭借自组装三维结构重现靶器官核心结构与功能,为相关研究提供独特平台。却因高度依赖天然生物支架而存在批次异质、成分不明、力学-生物信号难控等问题,阻碍模型标准化与实验可重复性,亦无法构建衰老组织特异性微环境。
肌肉骨骼衰老由多维度分子细胞事件驱动,其机制分为原发性标志(基因组不稳定、端粒缩短、表观遗传改变)、拮抗性标志(线粒体功能障碍、营养感应失调)与综合性标志(干细胞耗竭、慢性炎症、细胞外基质重塑),三者协同导致组织功能衰退。精准构建衰老肌肉骨骼类器官需采用系统性工程策略,细胞来源可选择带体内衰老特征的原代细胞或经基因编辑的干细胞,通过遗传操控、基因毒性应激、复制性衰竭及生物力学诱导等策略诱导衰老,同时需建立分子(SA-β-Gal、p16/p21、SASP)、功能(肌力、骨矿化、软骨力学)与系统(多组学、生物年龄量化)多维验证体系,该整合框架为体外研究肌肉骨骼衰老及筛选干预策略奠定生理相关性强的核心研究平台。
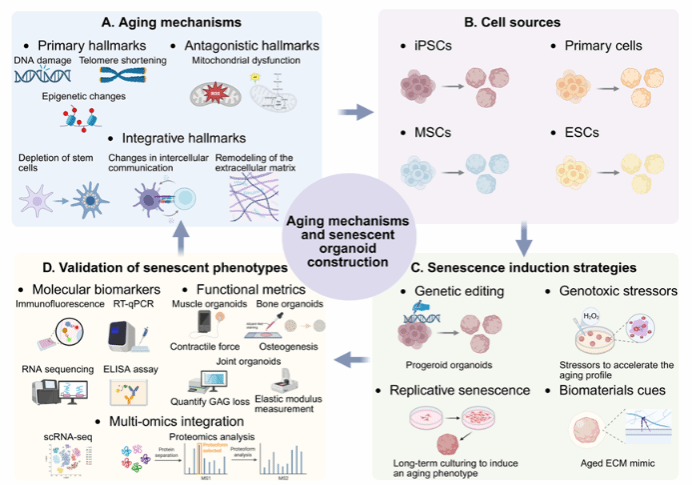
图1. 衰老机制与衰老类器官构建策略。 (A) 肌肉骨骼组织的核心衰老机制。(B) 用于构建衰老类器官的细胞来源。(C) 衰老诱导策略。(D) 衰老表型的验证。
肌肉骨骼衰老类器官构建中,精准调控生物工程材料的生化、力学、结构三大核心属性可系统性复现衰老微环境。
●生化层面通过调整胶原占比、降低糖胺聚糖含量模拟细胞外基质成分重塑,借助基质金属蛋白酶敏感或微图案化系统精准控释炎症因子与活性氧,诱导衰老相关分泌表型;
●力学层面以光交联调控水凝胶刚度模拟衰老组织硬化,经整合素- FAK/YAP 机械转导通路及表观遗传改变驱动细胞衰老,同时制备慢应力松弛粘弹性材料复现衰老组织机械记忆;
●结构层面调控支架孔隙率与拓扑结构,模拟骨质疏松相关高孔隙特征及胶原纤维紊乱排列,扰乱细胞机械感知以构建促衰老物理微环境。
综上,逆向工程调控材料关键参数,可构建高仿生、可调控的衰老类器官模型,为解析肌肉骨骼衰老机制与开展药物筛选提供理想研究平台。
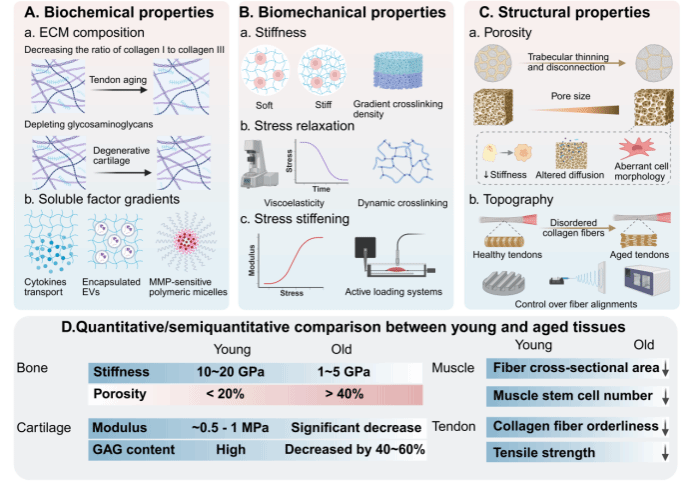
图2. 衰老微环境的关键材料参数调控。 (A) 生化性质调控。(B) 生物力学性质调控。(C) 结构性质调控。(D) 年轻与衰老组织材料性质的定量/半定量比较。
基于生物材料的肌肉骨骼衰老类器官模型虽已取得阶段性进展,但仍面临诸多关键挑战。
●现有模型长期稳定性欠佳,难以稳定维持衰老表型且无法精准复现体内细胞的异质性衰老特征;
●氧化应激等常用衰老诱导方法生理相关性有限,加之材料选型与构建方案缺乏统一标准,导致研究结果可重复性不足;
●同时模型体系完整性缺失,难以整合免疫、神经及血管等关键组分,限制对衰老微环境复杂细胞互作与信号调控的模拟能力;
●分析层面则普遍存在依赖终点检测、检测通量低、功能动态实时监测难等技术瓶颈。
未来,智能生物材料的动态自适应调控、多类器官整合与生物制造技术的多组织互联构建,结合人工智能助力的自动化标准化分析,将协同推动该类器官向高仿生度、高可控性方向迭代。
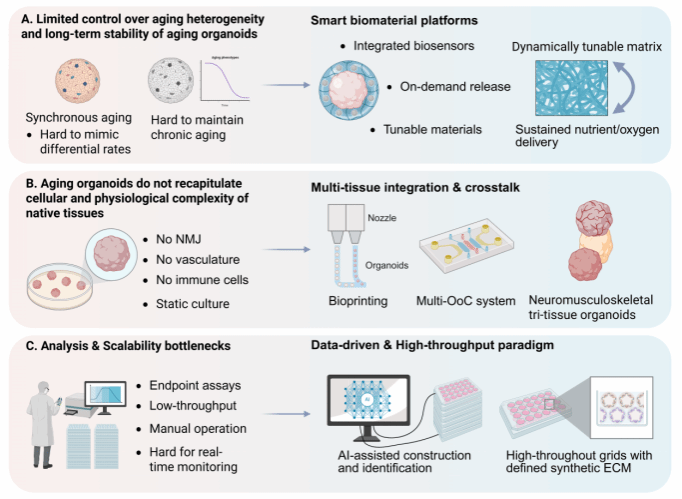
图3. 衰老类器官培养的现存局限与挑战应对策略。 (A) 对异质性和长期稳定性的控制有限(左),但可通过采用具有可调特性、集成生物传感器和按需释放系统的智能生物材料来改进(右)。(B) 细胞和生理复杂性不足(左),可通过多组织整合、多器官/神经肌肉骨骼系统的生物打印以及促进组织间通讯来克服(右)。(C) 分析和规模化瓶颈(左),例如低通量和实时监测有限,可通过数据驱动方法、AI辅助构建与识别以及采用合成ECM网格的高通量平台来解决(右)。


