近期,上海大学转化医学研究院/上海交通大学医学院附属新华医院骨科苏佳灿教授团队在期刊 BMEMat 上发表综述究性文章:"Artificial intelligence-enabled digital biomedical engineering"。此研究工作系统梳理了AI在医学影像分析、生物信号处理、生物材料设计以及新药研发等方向的代表性应用与典型案例,比较清晰地勾勒出数字生物医学工程的整体技术框架与应用版图。在总结现有应用的基础上,进一步讨论了大语言模型、多模态集成、智能实验室等新趋势在医疗文本处理、临床决策支持和自动化实验中的潜力,并分析数据隐私性、安全性等监管框架下的挑战。上海大学转化医学研究院宋沛然副研究员、唐璇博士、上海交通大学附属新华医院吕旭昆同学为论文共同第一作者,上海大学转化医学研究院/上海交通大学医学院附属新华医院苏佳灿教授、上海大学转化医学研究院白龙研究员、上海交通大学医学院附属新华医陈晓副主任医师后为论文共同通讯作者。
研究背景
随着人工智能在计算性能、模式识别和大规模数据处理方面的持续突破,生命科学与医学领域逐渐迈入以数据和模型为核心驱动力的新时代。传统生物医学工程长期依赖经验驱动的小样本实验和常规实验室流程,在复杂疾病早期筛查、个体化诊疗方案制定、新型生物材料和药物的高效开发等方面日益暴露出效率低、周期长、可扩展性有限等局限。
在此背景下,将机器学习、深度学习、计算机视觉、自然语言处理及多模态学习等AI技术系统性引入生物医学工程,催生了以数据驱动和智能决策为特征的数字生物医学工程。数字生物医学工程强调结合AI技术、大数据分析与计算建模,构建可支持智能诊断、预测评估和个体化干预的数字化研究与应用体系。文章在全面回顾传统生物医学工程发展脉络与主要挑战的基础上,系统梳理AI在医学影像分析、生物信号处理、生物材料设计及新药研发等关键方向的代表性进展,同时回应数据隐私、模型可解释性与监管合规等现实问题。
文章摘要
人工智能(AI)已成为生物医学工程领域的一股变革力量,催生了向数据驱动、智能化研究范式的转变。凭借其在计算、模式识别和大规模数据分析方面的先进能力,AI显著提高了生物医学研究的效率、精度和可重复性。特别是AI与生物医学工程的融合,催生了“数字生物医学工程”这一新兴领域,该领域强调整合AI技术、大数据分析和计算建模,以在生命科学领域实现智能化、预测性和个性化的解决方案。本综述全面概述了AI在生物医学工程中的应用现状,重点介绍了医学图像分析、生物信号处理、生物材料设计和药物开发方面的进展。文章还强调了AI如何提高诊断精度、加速材料和药物发现,并促进个性化和预测性医疗。此外,本文还讨论了AI应用的局限性和监管挑战,同时概述了未来的方向,以指导数字生物医学时代的科研创新和临床转化。
综述架构与方法
本文通过广泛的文献调研,构建了从底层AI算法到上层生物医学应用场景的完整知识图谱,系统梳理了该领域的演进路径。
核心技术层: 详细解析了机器学习(ML)、深度学习(DL)、计算机视觉(CV)、自然语言处理(NLP)及大语言模型(LLMs)等AI核心算法在生物医学中的技术原理。
应用场景一(医学影像): 分析了AI在肺癌、乳腺癌、脑转移瘤等疾病筛查中的应用,重点关注卷积神经网络(CNN)在提高诊断敏感性和特异性方面的表现。
应用场景二(生物信号): 探讨了AI在心电图(ECG)、脑电图(EEG)及多模态信号融合中的应用,展示了其在实时监测和疾病预警中的价值。
应用场景三(材料与药物): 阐述了生成式模型如何通过逆向设计加速生物材料的发现,以及AlphaFold等工具如何革命性地改变蛋白质结构预测与新药筛选流程。
伦理与挑战: 深入讨论了数据隐私、算法黑箱、伦理责任归属及监管合规性等关键问题,并提出了建立标准化数据集和国际合作框架的建议。
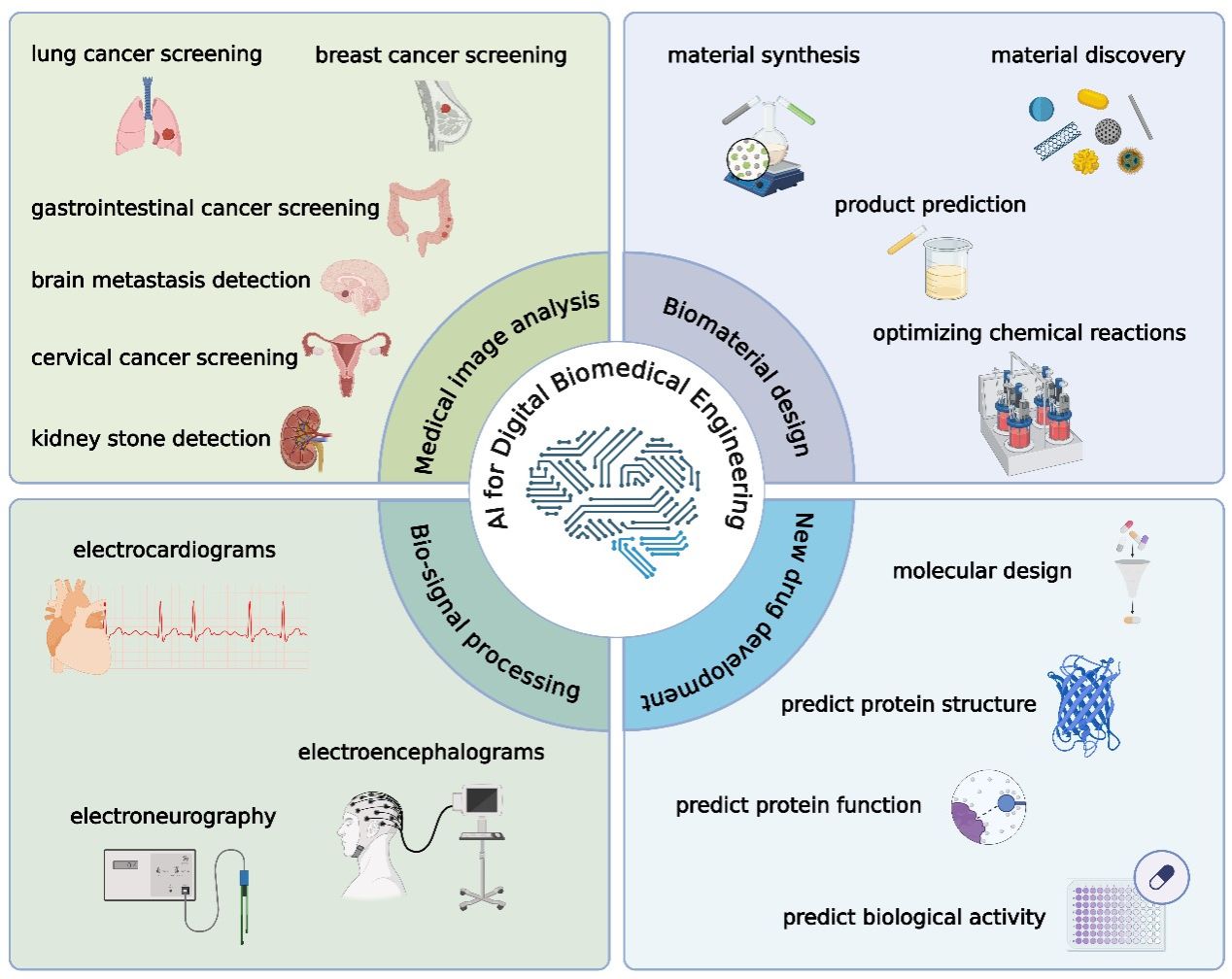
图1:AI在生物医学工程中的代表性应用。
涵盖医学图像分析(如肺癌、乳腺癌筛查)、生物信号处理(如心电图、脑电图)、生物材料设计(如材料合成、性能预测)及新药开发(如分子设计、蛋白质结构预测)。AI正赋能数字生物医学工程的各个维度。

图2:AI技术应用概览。
(a) 利用深度学习框架支持医疗机构的临床操作;(b) 基于流动化学原理的自动化平台;(c) 利用AI推进基于天然产物的药物发现;(d) AI模型应用于材料开发与选择、工艺模拟、性能预测及全生命周期预后;(e) 模块化分子设计;(f) AI和深度学习在药物发现中的应用。
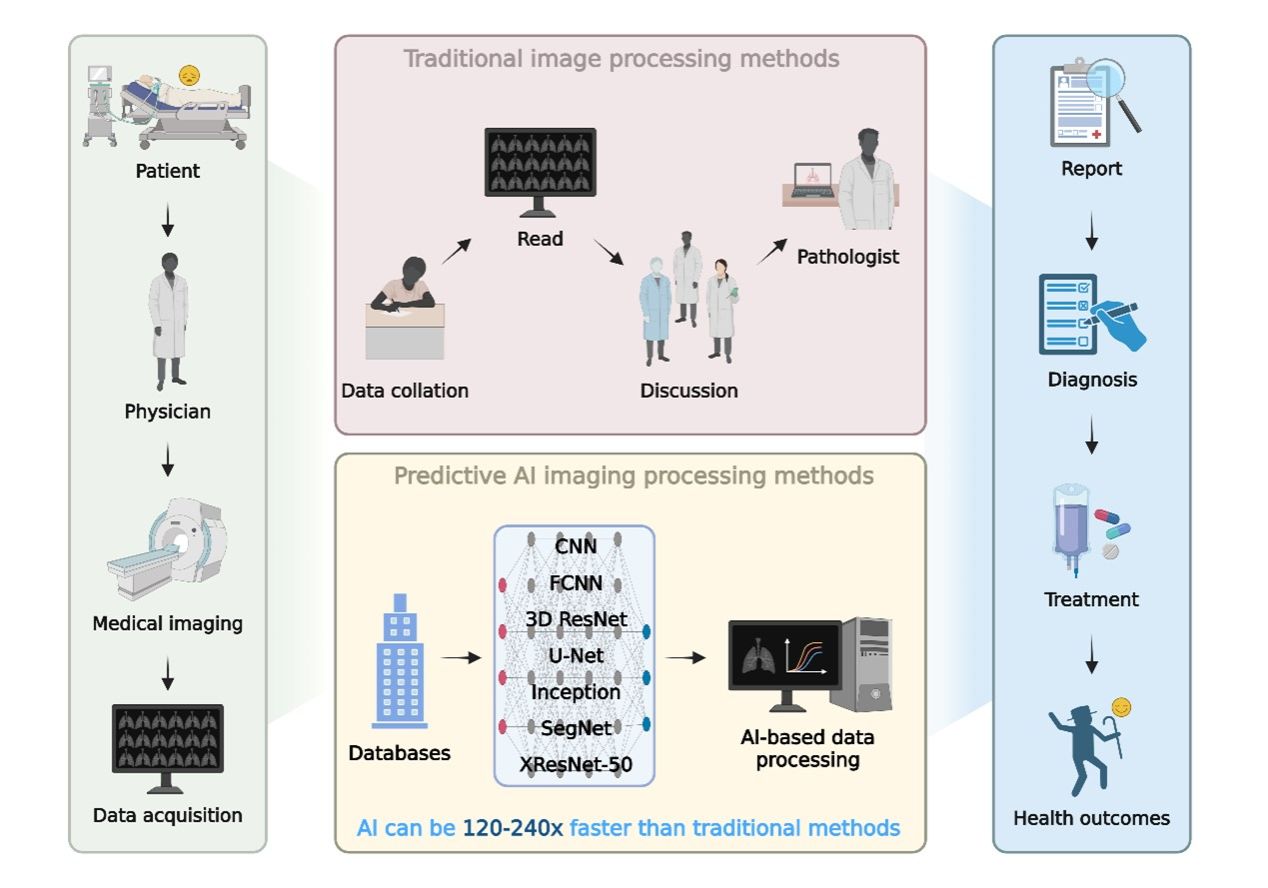
图3:AI在医学图像分析中的表现优于传统方法。
对比了传统图像处理流程(依赖人工阅读、讨论、诊断)与预测性AI图像处理方法(基于数据库、CNN/ResNet等深度模型进行数据处理),AI在速度上可比传统方法快120-240倍,并能显著改善健康结果。
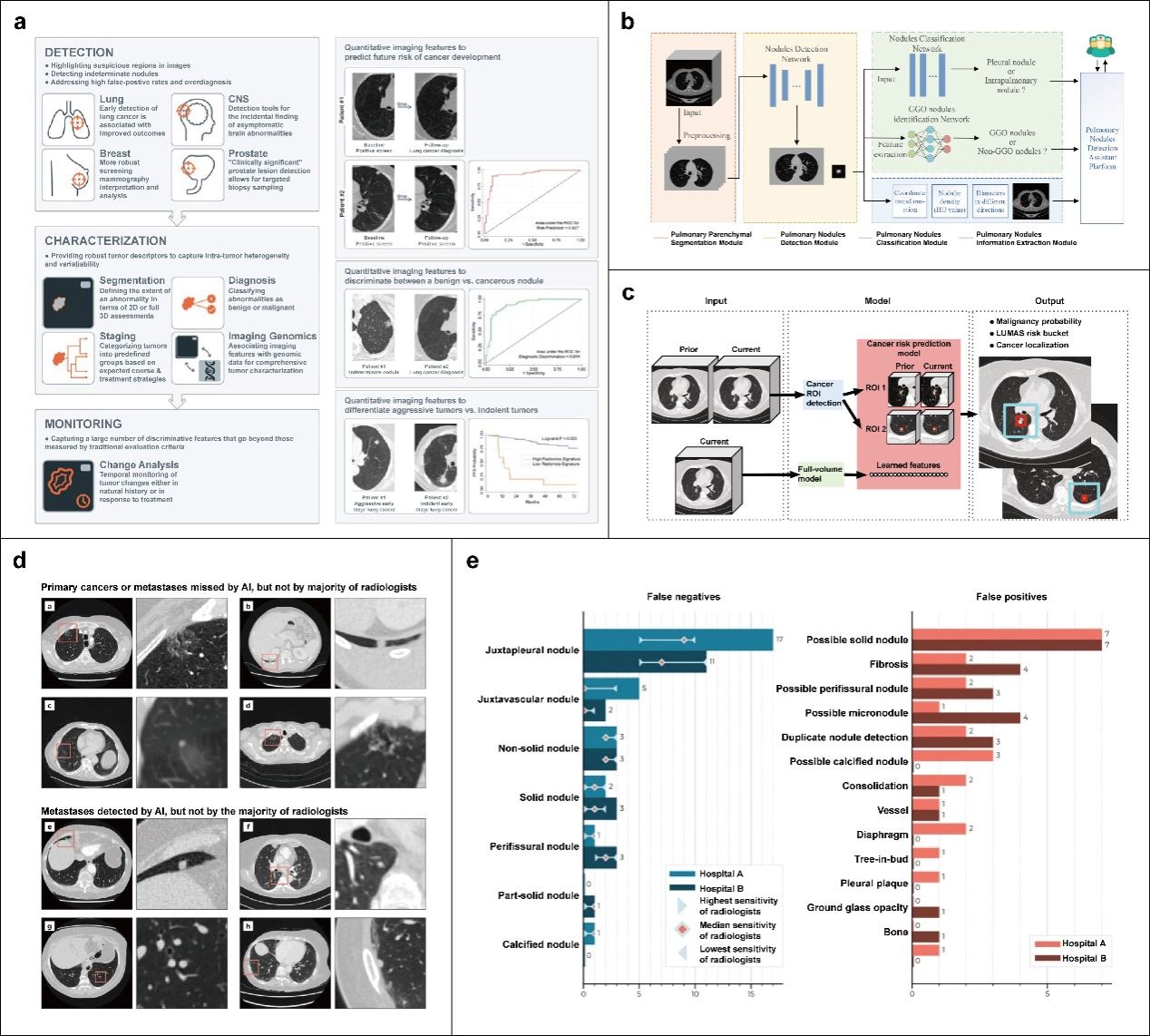
图4:AI在肺癌筛查中的应用。
(a) AI在肺结节初次检测时预测肺癌风险;(b) 专为肺结节分析设计的架构辅助平台;(c) 用于肺癌筛查的三维深度学习模型;(d) AI系统识别出的原发性肿瘤和肺转移瘤(部分被放射科医生漏诊);(e) AI系统在肺癌检测中的假阴性和假阳性分类分布模式。
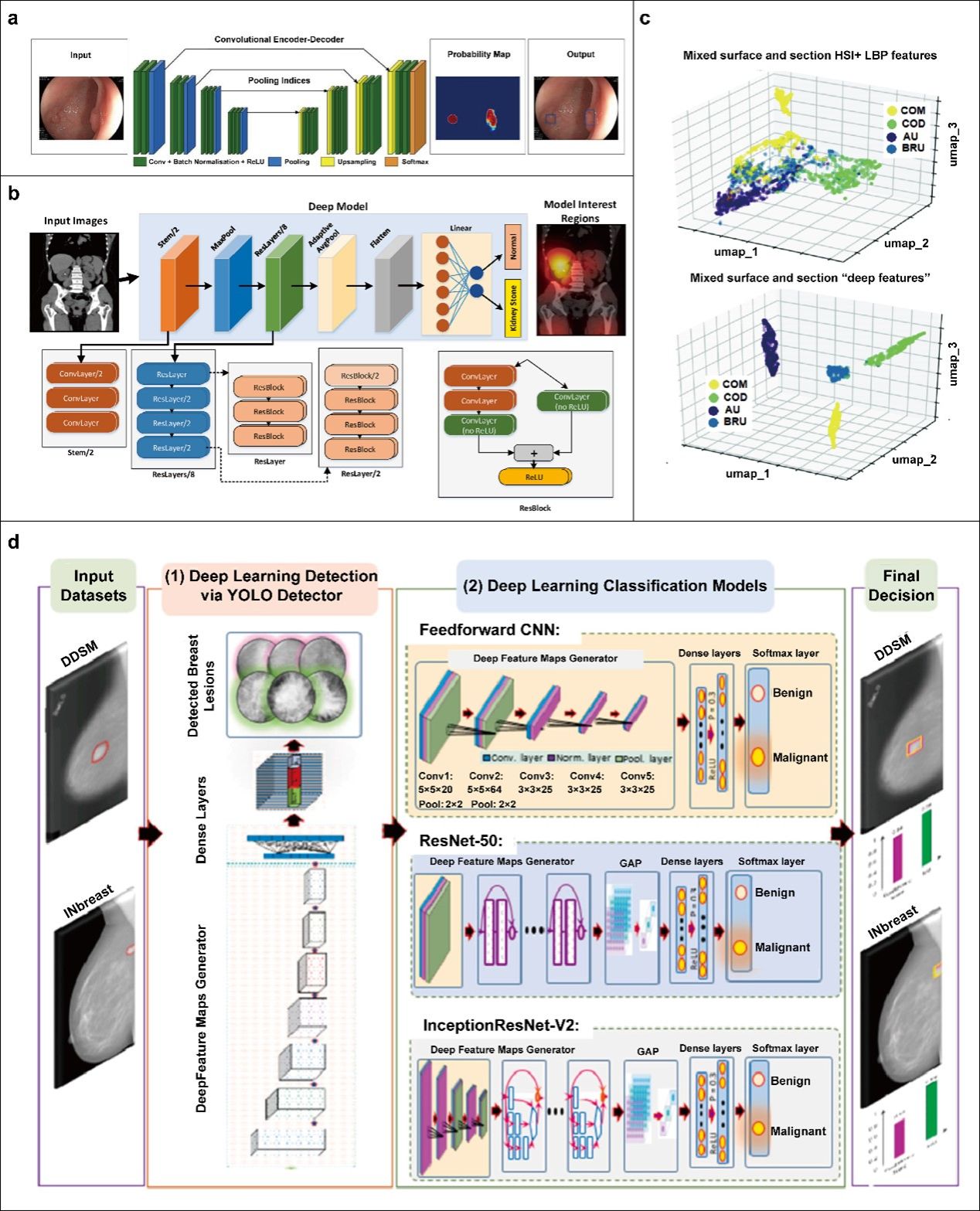
图5:AI在多部位疾病检测中的应用。
(a) 深度学习模型应用于结肠镜图像分析;(b) 基于XResNet-50深度学习架构的肾结石自动检测;(c) 深度学习模型支持通过内窥镜成像评估肾结石;(d) 深度学习用于乳腺病变的检测与分类。
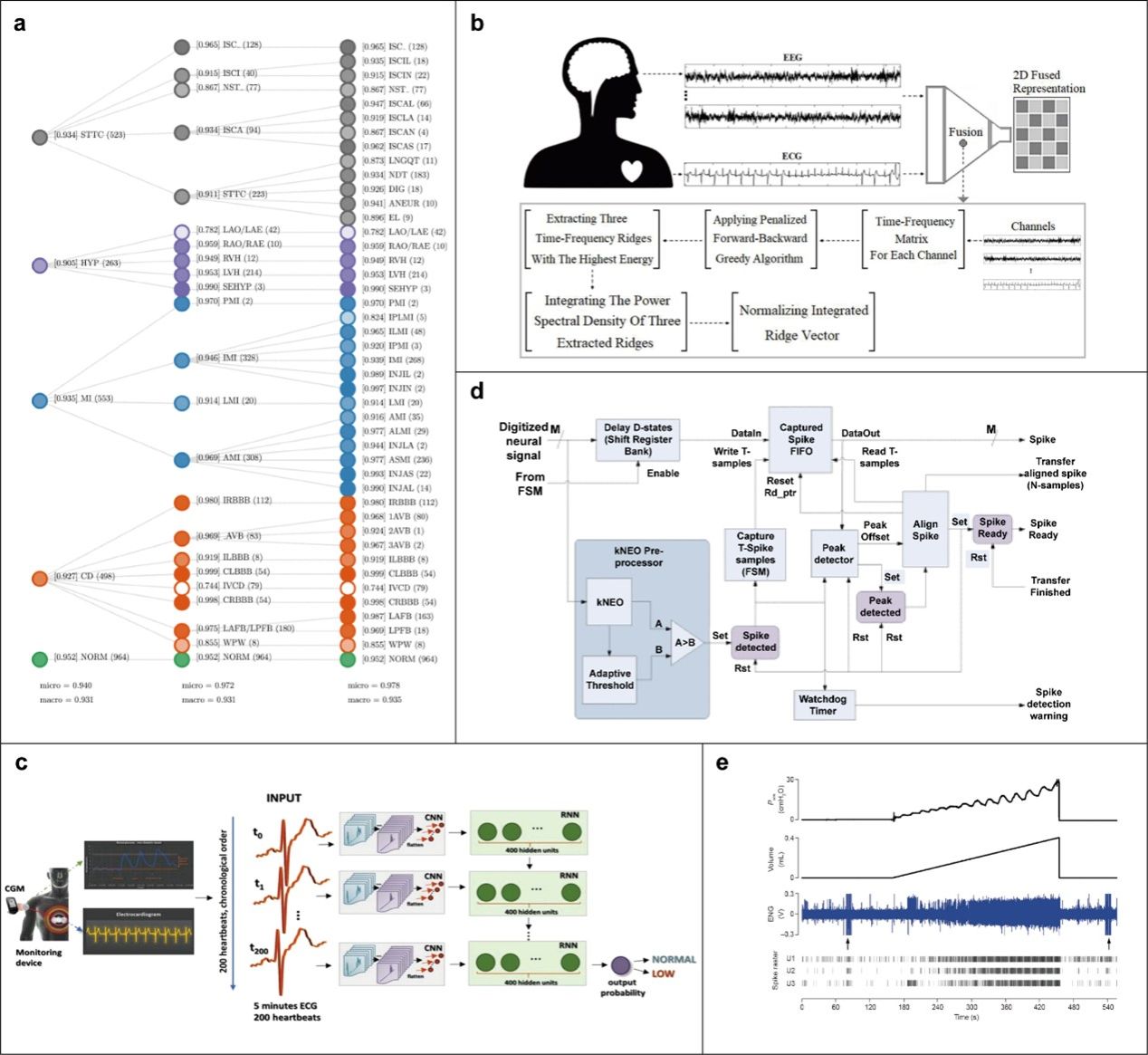
图6:AI在生物信号处理中的应用。
(a) 用于分析心电图数据的深度学习方法;(b) 结合时频脊映射与深度学习架构监测麻醉期间的生理状态;(c) 开发结合CNN和RNN的系统以识别5分钟内的低血糖发作;(d) 设计用于通过传入神经通路监测膀胱容量的数字信号处理器(DSP);(e) 监测传入神经活动以检测膀胱容量和压力的变化。
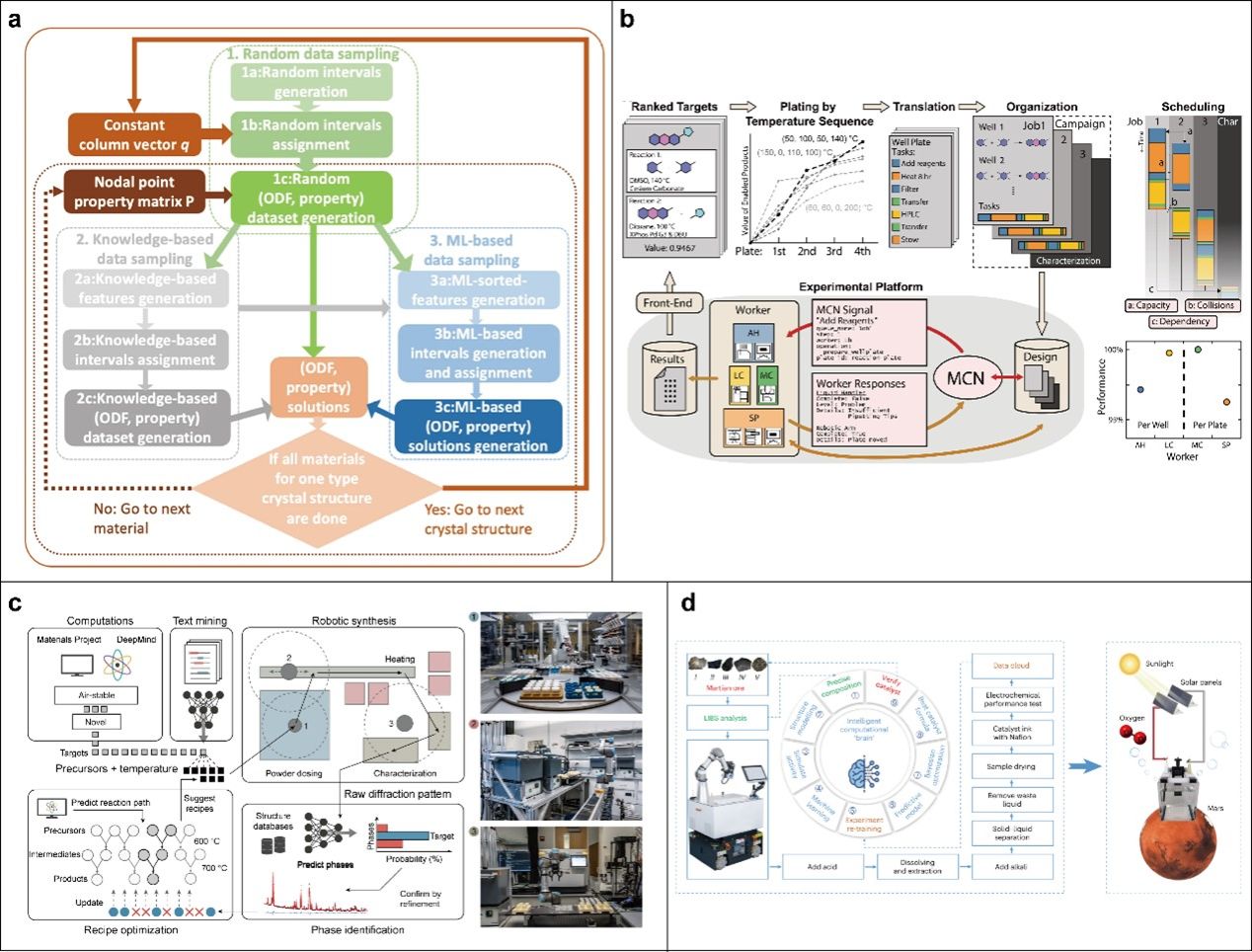
图7:AI赋能材料设计与合成。
(a) AI赋能的材料微观结构优化;(b) “设计-制造-测试-分析”工作流,无需人工实验即可探索化学结构;(c) A-Lab平台通过自动化实现新材料的自主发现;(d) “AI化学家”设计并合成电催化剂。
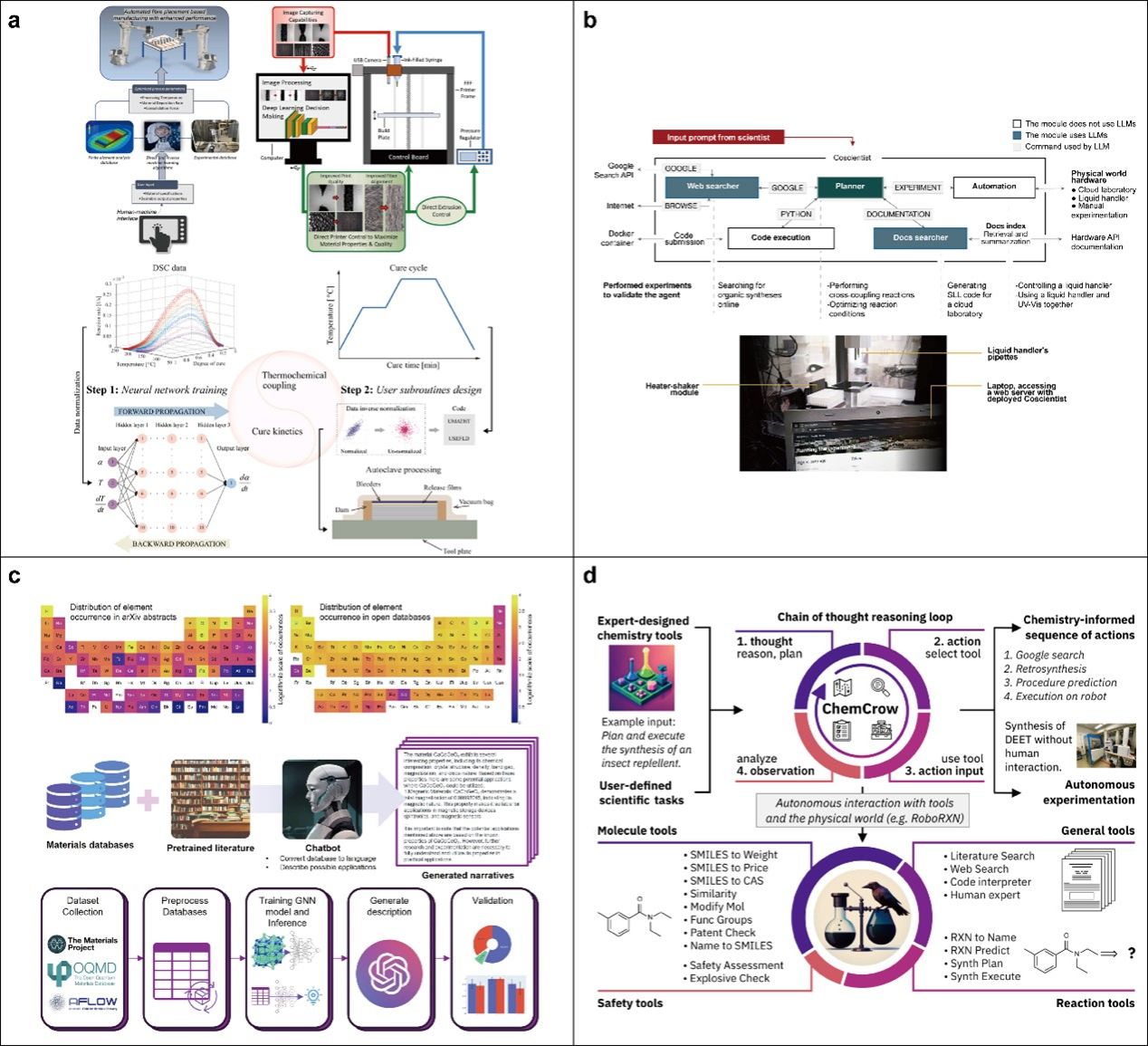
图8:AI在先进制造与化学实验中的应用。
(a) 机器学习技术用于增强先进复合材料的设计与性能优化;(b) 通过Opentrons Python API和符号实验室语言(SLL)促进自动化化学实验;(c) 多模态数据源与大语言模型结合,促进固态材料的探索与识别;(d) ChemCrow作为多功能平台,能够执行有机合成、药物开发及先进材料设计的工作流。
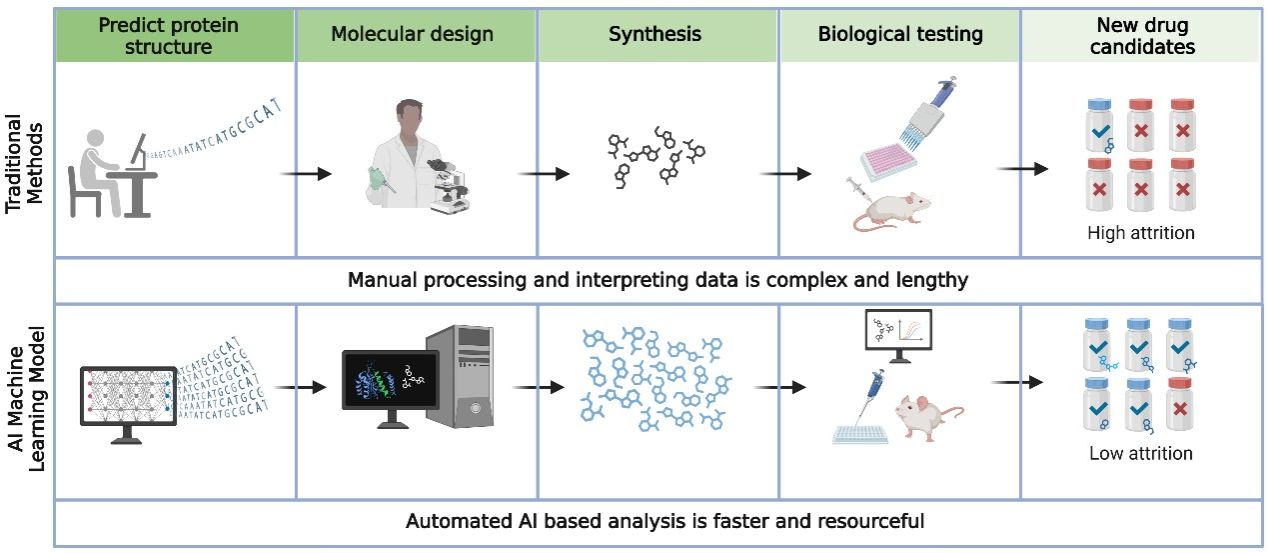
图9:AI用于药物设计。
对比了传统方法(高损耗、流程长)与AI机器学习模型(低损耗、自动化分析),展示了AI在预测蛋白质结构、分子设计、合成及生物测试全流程中的优势。
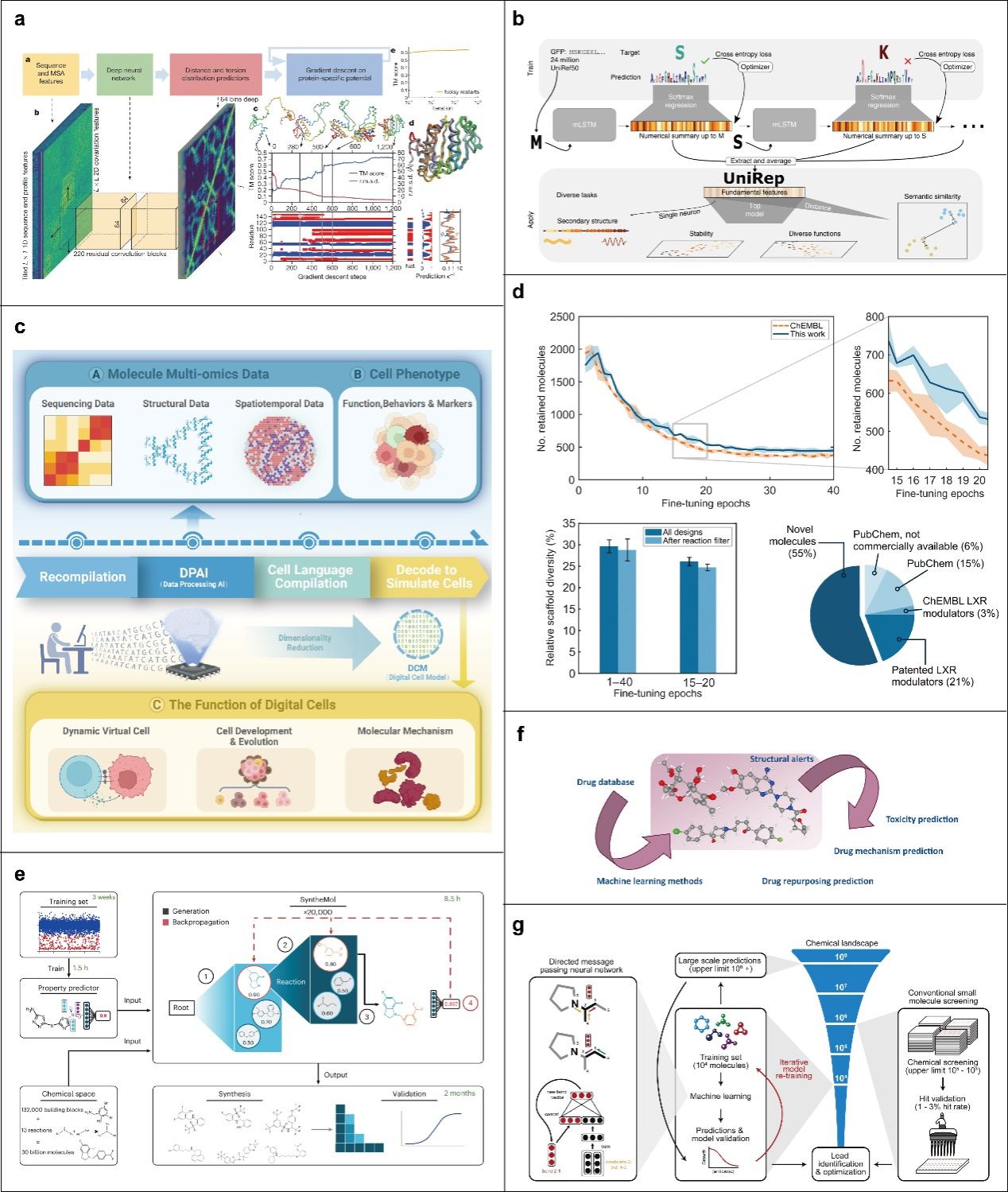
图10:AI在蛋白质工程与药物发现中的前沿应用。
(a) 应用深度学习技术预测蛋白质三维结构(如AlphaFold);(b) 统一表示模型(UniRep)显著提高蛋白质工程效率;(c) 数字细胞模型;(d) 使用深度学习技术自动化化合物设计;(e) 利用生成式AI技术SyntheMol开发新型抗生素;(f) 机器学习方法用于增强药物设计策略;(g) 利用机器学习进行抗生素发现(如Halicin的发现)。
总结与展望
在人工智能的加持下,数字生物医学工程不只是提升算法性能,而是在重新塑造生物医学工程的技术基础和研究模式,为构建更加精准、智能和可持续的未来医疗体系提供关键支撑。通过将机器学习、深度学习、多模态大模型等技术系统嵌入医学影像、生物信号、生物材料与新药研发等关键环节,数字生物医学工程正在推动疾病认知从静态表征走向动态演化与机制解析,推动临床决策从经验驱动走向数据驱动与证据融合。
面向未来,随着多模态大模型、数字孪生和智能实验室等新范式的不断成熟,数字生物医学工程有望在数字化病人构建、个体化干预策略优化以及虚拟试验与真实世界证据融合等方面发挥更大作用。同时,数据隐私保护、算法可解释性、公平性评估及监管规范等问题也将持续塑造这一新兴领域的发展边界。只有在技术创新与伦理监管双轮驱动下,构建起开放共享而又安全可控的科研与临床应用生态,数字生物医学工程才能真正实现从概念框架走向临床实践,为人类健康提供更加高效、可及与负责任的解决方案。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/bmm2.70049

