近日,Organoid research期刊在线发表上海大学苏佳灿教授团队最新综述《Organoid-derived extracellular vesicles: From organoid, to organoid》。该文章系统梳理类器官的发展历程、基本概念、构建方法及应用场景,概述其类型、研究进展与独特优势;同时阐述细胞外囊泡的基本生物学特性及其在疾病治疗与干预中的潜在价值,并重点剖析类器官来源的细胞外囊泡(Organoid-derived extracellular vesicles,OEVs)与传统细胞外囊泡核心差异。本文总结OEVs优势与当前面临的挑战,有望加速其在疾病治疗领域的临床转化。
文章信息
题目:Organoid-derived extracellular vesicles: From organoid, to organoid
作者:Ting Cheng, Wojciech Chrzanowski*, Han Liu*, Jiacan Su*
引用信息:Ting Cheng, Wojciech Chrzanowski, Han Liu, Jiacan Su. Organoid-derived extracellular vesicles: From organoid, to organoid. Organoid Res., 2025, 1(4), 025450031. https://doi.org/10.36922/OR025450031
文章链接:
https://accscience.com/journal/OR/1/4/10.36922/OR025450031
文章简介
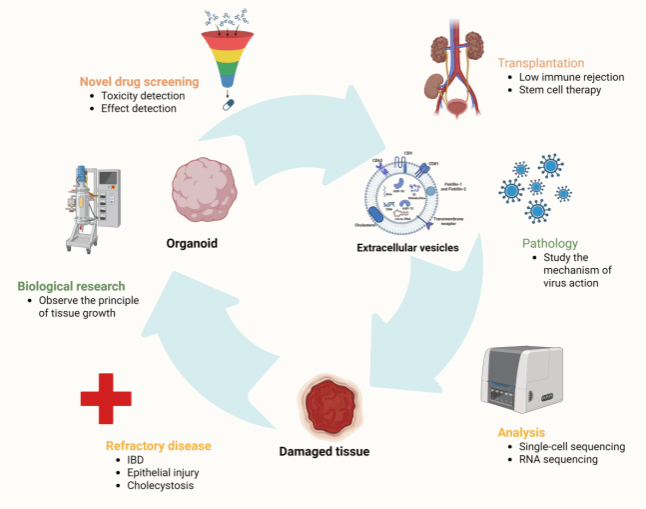
类器官是在体外培养形成的三维微生理系统,能够模拟真实器官的结构与功能,在疾病建模和再生医学中应用广泛。
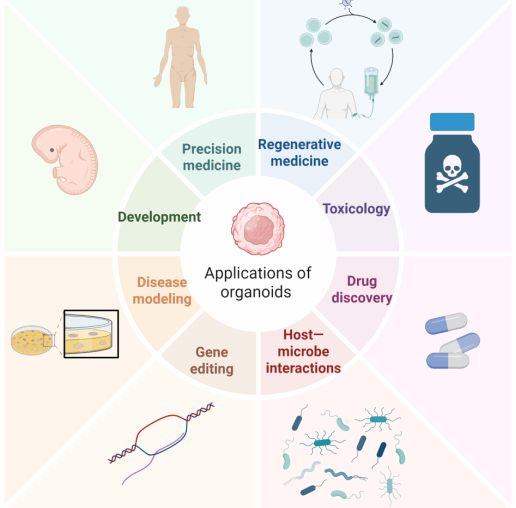
类器官技术多领域应用全景
与此同时,细胞外囊泡作为细胞间通信的关键纳米信使,因其良好的生物相容性和递送潜力而备受关注。本文系统性地提出“从类器官到类器官”的闭环研究范式,并强调类器官微环境特异性是决定其来源细胞外囊泡分子组成与功能优势的核心,为发展“个性化外泌体治疗”和“原位再生诱导”奠定理论基础。与传统二维培养或简单三维培养产生的细胞外囊泡相比,类器官来源的细胞外囊泡(Organoid-derived extracellular vesicles,OEVs)具有显著优势。由于类器官具备复杂的多细胞结构、细胞间相互作用以及更接近体内的生理微环境,其所分泌的囊泡负载更为丰富且特异的蛋白质、核酸与脂质分子,形成独特的“分子指纹”。
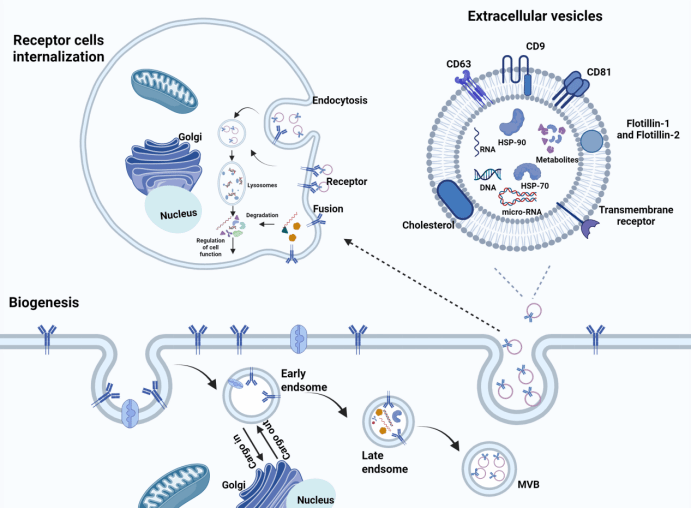
OEVs在类器官复杂微环境中的生物发生途径
这些囊泡不仅产量更高、膜结构更有序,而且表现出更强的生理活性和组织调控能力,在促进神经修复、血管生成和免疫调节方面效果显著。在应用层面,类器官来源的细胞外囊泡展现出巨大的转化潜力。研究表明,其在肠道炎症调控、唾液腺上皮修复、皮肤伤口愈合及视网膜保护等疾病过程中发挥重要作用,疗效甚至优于母体类器官的直接移植。同时,凭借其天然的纳米尺度、低免疫原性与跨越生理屏障的能力,它们可作为智能药物载体,实现化疗药物、核酸或蛋白的靶向递送,为肿瘤治疗和遗传性疾病提供新策略。
尽管前景广阔,类器官来源细胞外囊泡的发展仍面临规模化制备、标准化提取、作用机制解析以及质量控制等挑战。未来研究需聚焦于通过工程化改造、生物反应器规模化培养、多组学与人工智能整合分析等手段,推动其向可控、高效、标准化的“下一代生物疗法”演进。这类囊泡有望与基因治疗、组织工程深度融合,为退行性疾病、器官损伤及个性化医疗提供突破性解决方案。
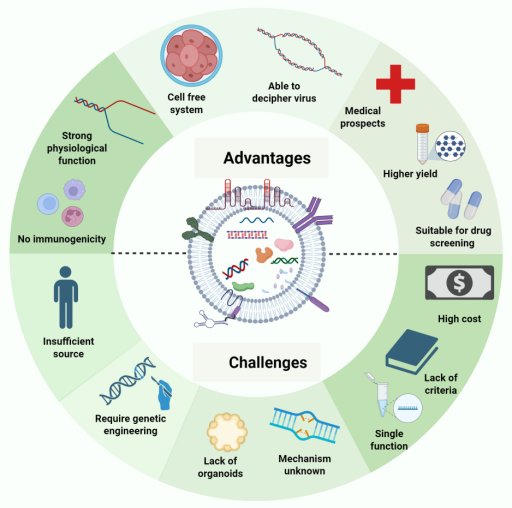
类器官来源细胞外囊泡的优势与挑战
研究意义
展望未来,尽管OEVs在转化应用中仍面临制备、标准化与机制解析等挑战,但随着生物技术、纳米医学与人工智能的交叉融合,其发展前景广阔。在载体工程方面,借助基因编辑与合成生物学技术对亲本类器官进行改造,或对OEVs进行表面修饰与载荷设计,能够赋予其靶向递送、可控释放及免疫调节等智能化功能,从而实现对疾病微环境的精准干预。在规模化与标准化方面,结合3D生物打印等先进制造技术,构建稳定可控的类器官培养平台,并建立从细胞源、培养条件到囊泡分离、鉴定的全流程标准化体系。通过多组学分析与人工智能整合,解析OEVs的“分子指纹-功能图谱”,将推动其在个性化治疗、疾病模型构建及再生医学中的广泛应用,为突破传统治疗局限、实现“原位再生”提供全新的生物技术策略。


