近日,Organoid research期刊在线发表中国人民解放军总医院第四医学中心彭江教授团队研究性论文《Self-Organizing Vascularized Subchondral Bone Organoids from Stromal Vascular Fraction Enable Functional Osteochondral Interface Regeneration》。该研究构建一种基于脂肪来源基质血管组分(SVF)与去细胞化软骨基质(CECM)的自组织血管化软骨下骨类器官(SSBO),系统重建软骨–骨界面的血管、免疫与成骨耦合微环境,为骨关节炎机制研究、骨软骨缺损修复及再生医学提供全新的类器官模型与可转化技术路径。
文章信息
题目:Self-organizing vascularized subchondral bone organoids from stromal vascular fraction enable functional osteochondral interface regeneration
作者:Tao Qian, Jiazhou Wu, Zexian Liu, Aiyuan Wang, Yanbin Wu, Junli Wang, Hongyu Jiang, Zhengrui Zhou, Cheng Huang, Yazhou Li, Junming Zhang, Biao Ma, Yun Bai, Jialiang You, Endong Luo, Dingkai Wang, Ying He*, Jiang Peng*
引用信息:Tao Qian, Jiazhou Wu, Zexian Liu, et al. Self-organizing vascularized subchondral bone organoids from stromal vascular fraction enable functional osteochondral interface regeneration. Organoid Res, 2025, 1(4), 025480037. https://doi.org/10.36922/OR025480037
文章链接:https://accscience.com/journal/OR/1/4/10.36922/OR025480037
文章简介
软骨下骨是关节稳态维持和骨关节炎(OA)发生发展的关键结构单元。近年来研究发现,SCB 的异常重塑、血管异常生成及免疫微环境失衡往往早于软骨退变发生,并通过“骨–血管–免疫”耦合机制加速疾病进展。然而,现有二维细胞模型或单一细胞来源的三维构建体系,难以同时模拟 SCB 的多细胞组成、空间结构及动态功能特征,严重限制其在疾病建模与再生修复中的应用价值。
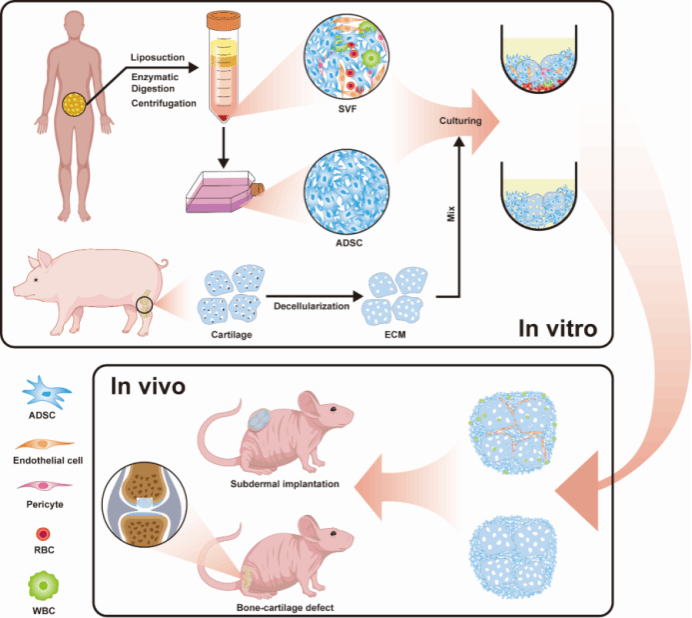
本研究提出并构建一种自组织软骨下骨类器官(SSBO)。该体系以SVF作为多细胞来源,联合CECM作为天然支架,在无外源生长因子条件下实现自发聚集、自组织与多谱系分化。SVF 中富含脂肪干细胞、内皮祖细胞、周细胞及免疫细胞,为类器官提供内在的细胞异质性与功能协同基础;CECM 则保留软骨特异性结构与生化信号,为类器官发育提供接近生理状态的微环境。
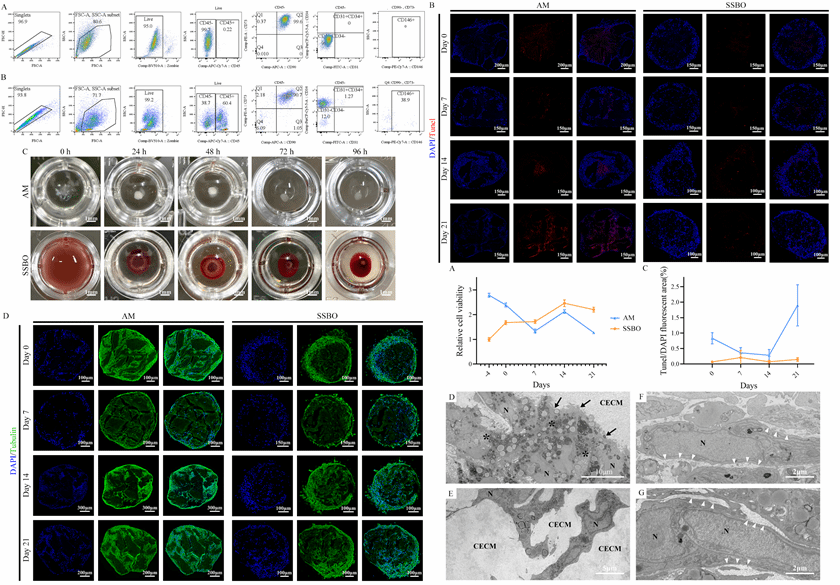
图1:类器官构建及表征
在体外培养过程中,SSBO 展现出显著优于单一 ADSC 构建体系的生物学特性。多细胞协同作用促进细胞向基质内部主动迁移,并伴随显著的基质降解与再沉积,形成高度整合的三维结构。超微结构与分子分析显示,SSBO 内部发生类似软骨内成骨的连续分化过程:早期表达 SOX9 与 COL2A1,随后依次上调 RUNX2、COL1A1 与 OCN,提示其在时间和空间上高度模拟生理性软骨向骨转变路径。
尤为重要的是,SSBO 在无额外血管诱导条件下,自发形成结构清晰的血管样网络。SVF 中的内皮祖细胞沿 CECM 排列形成管腔样结构,周细胞呈伴行分布,构建出稳定的类血管系统。与此同时,巨噬细胞在类器官形成早期短暂激活炎症反应,随后快速向 IL-10 主导的抗炎表型转变,维持有利于组织重建的免疫微环境,揭示免疫调控在类器官自组织与稳定中的关键作用。
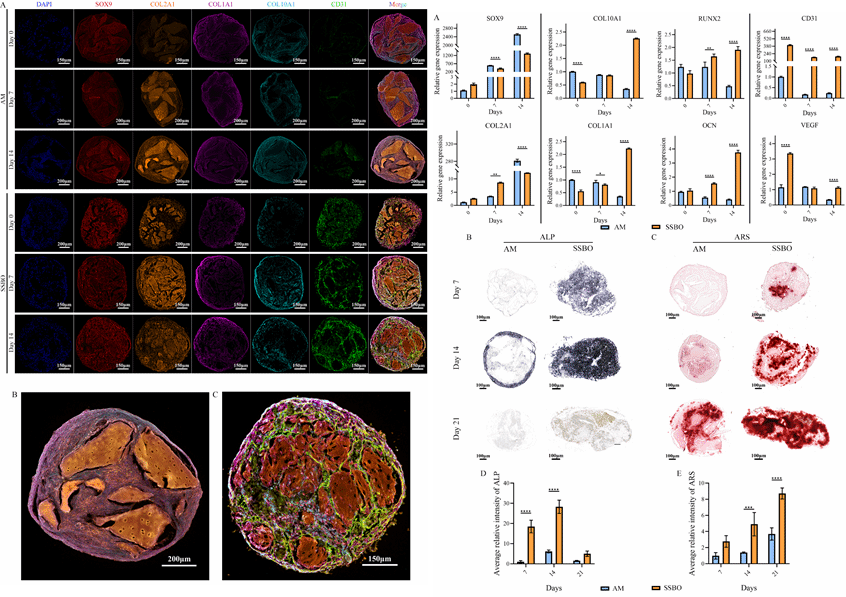
图2:类器官内细胞的空间分布及分化
在体内实验中,SSBO 表现出优异的血管整合与成骨能力。皮下移植后,类器官可与宿主血管系统形成嵌合血管网络,并生成结构有序的骨样组织。在小鼠骨软骨缺损模型中,SSBO 显著促进软骨下骨重建与上覆软骨再生,在骨体积、骨小梁结构及组织学评分等多项指标上均优于对照组,修复效果接近正常关节组织。
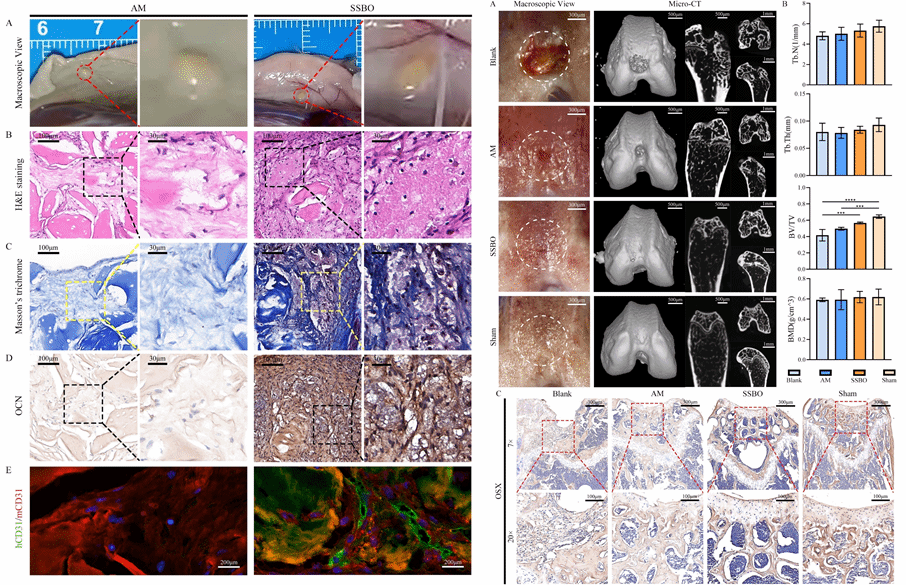
图3:各种肿瘤来源类器官建立及其临床应用
总体而言,本研究构建的 SSBO 类器官不仅在结构与功能层面高度模拟真实软骨下骨微环境,还兼具血管生成、免疫调控与成骨分化等关键特性,为骨关节炎早期机制研究、骨软骨界面再生及个体化修复策略提供全新的实验平台与潜在临床转化方案。
作者简介
彭江,中国人民解放军总医院第四医学中心骨科医学部研究所所长,博士生导师。长期从事骨科战伤救治及再生医学基础与临床应用研究。现为国家重点研发计划干细胞专项项目首席科学家,主持国家重点研发计划课题1项、国家自然科学基金项目1项、军队重点课题3项,项目总经费累计5400余万元。已发表SCI论文160余篇,近三年以通讯作者或共同通讯作者身份发表SCI论文45篇,授权发明专利12项,H指数56。


